Embrüonaalsed tüvirakud
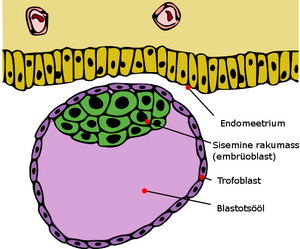
Embrüonaalsed tüvirakud on pluripotentsed tüvirakud, mis on saadud embrüo varajase staadiumi blastotsüsti sisemisest rakumassist. Inimese embrüo jõuab blastotsüsti staadiumisse 4–5 päeva pärast viljastumist, koosnedes ligikaudu 50–100 rakust. Inimese embrüonaalsete tüvirakkude saamine püstitab palju eetilisi probleeme, sest viljastatud munarakk hävineb sisemise rakumassi isoleerimisel.

Omadused
Teadustöös enimkasutatavate inimese ja hiire embrüonaalsete tüvirakkude diameeter on vastavalt ligikaudu 14 ja 8 μm. Embrüonaalseid tüvirakke iseloomustab nende kaks eriomadust:
- pluripotentsus,
- võime paljuneda lõputult.
Embrüonaalsed tüvirakud on pluripotentsed, mis tähendab, et nad suudavad diferentseeruda kõikideks primaarseteks lootelehtedeks: välimine (ektoderm), keskmine (mesoderm) ja sisemine (endoderm). Täiskasvanud inimese kehas kuulub igasse lootelehte rohkem kui 220 rakutüüpi. Pluripotentsus eristabki embrüonaalsed tüvirakke täiskasvanu (somaatilistest) tüvirakkudest, sest embrüonaalsed tüvirakud panevad aluse kõigile keharakutüüpidele, kuid somaatilised tüvirakud on multipotentsed ehk nende diferentseerumisvõime on piiratud.
Spetsiifilises kasvukeskkonnas säilitavad embrüonaalsed tüvirakud oma piiramatu jagunemisvõime. See võimaldab embrüonaalseid tüvirakke kasutada edukalt teadustöös ja loodetavasti ka tuleviku meditsiinilises taastusravis.
Arvatakse, et embrüonaalsete tüvirakkude plastilisust ja potentsiaali piiramatuks paljunemiseks saab kasutada taastusravis ja vigastatud või haigete kudede asendamiseks. Meditsiinis võiks pluripotentsete tüvirakkude abil ravida palju vere ja immuunsüsteemiga seotud haigusi ja häireid, vähkkasvajaid, laste diabeeti, Parkinsoni tõbe ja selgroovigastusi. Lisaks tüvirakuteraapia eetilistele probleemidele, on teiselt inimeselt (allogeensel) tüvirakkude siirdamisel takistavaks teguriks ka doonori ja vastuvõtja sobimatus. Koesobivuse probleemi lahendamisel võivad abiks olla inimese enda somaatiliste tüvirakkude kasutamine, terapeutiline kloonimine, tüvirakupangad või kindlate faktoritega reprogrammeeritud somaatiliste rakkude kasutamine (indutseeritud pluripotentsed tüvirakud). Embrüonaalseid tüvirakke kasutatakse ka inimese varajase arengu ja geneetiliste haiguste uurimiseks ning in vitro süsteemina toksikoloogilistes katsetustes.
Uuringute ajalugu
1964. aastal eraldati teratokartsinoomist, mis oli sugurakkudest tekkinud kasvaja, kindel rakutüüp. Need teratokartsinoomist eraldatud rakud paljunesid ja kasvasid rakukultuuris nagu tüvirakud ja on tänapäeval tuntud kui embrüonaalse vähi rakud. Sarnase välimuse ja diferentseerumise potentsiaali (pluripotentsus) tõttu hakati embrüonaalse kartsinoomi rakke kasutama hiire varajase arengu in vitro mudelina. Teratokartsinoomi arengu jooksul tekivad embrüonaalse kartsinoomi rakkudes geneetilised mutatsioonid ja ebanormaalne karüotüüp. Sellised geneetilised kõrvalekalded tekitasidki vajaduse normaalsete pluripotentsete rakkude eraldamiseks blastotsüsti sisemisest rakumassist.
1981. aastal eraldati esimest korda hiire embrüonaalsed tüvirakud kahes erinevas teadustöörühmas. Martin Evans ja Matthew Kaufman Cambridge'i Ülikooli geneetika osakonnast avaldasid juulis uue protseduuri, mis võimaldas kasvatada hiire embrüoid emakas, suurendades rakkude arvu ja saades embrüost embrüonaalsed tüvirakke. Gail R. Martin San Francisco California Ülikooli anatoomia osakonnast avaldas oma artikli detsembris ja mõtles välja termini "embrüonaalne tüvirakk". Ta näitas, et embrüoid saab ka in vitro kasvatada ning hiljem saab neist ka embrüonaalseid tüvirakke. 1998. aastal toimus aga läbimurre, sest James Thomsoni juhitud Wisconsin-Madisoni Ülikooli teadlased olid esimesed, kes töötasid välja metoodika inimese embrüonaalsete tüvirakkude isoleerimiseks ja kasvatamiseks rakukultuuris.
Embrüonaalsete tüvirakkude saamise ja kasvatamise meetodid ja tingimused
Inimese embrüonaalsete tüvirakkude saamine. In vitro viljastamise protseduuris kasutatakse algselt mitmeid munarakke ja tekkinud embrüotest valitakse välja parimad. Ülejäävaid embrüoid, mida kliiniliselt ei kasutata või mis on sobimatud implantatsiooniks patsienti, saab doonori nõusolekul annetada. Nendest annetatud embrüotest, mis muidu hävitataks, saadaksegi inimese embrüonaalsed tüvirakud. Blastotsüstistaadiumis olevast embrüost eraldatakse sisemine rakumass, kasutades mehaanilist lahkamist ja immunokirurgiat. Saadud sisemine rakumass pannakse kasvama abirakkudele ehk toiterakkudele. Sisemise rakumassi rakud kinnituvad ja jagunevad veelgi, moodustades inimese embrüonaalsed diferentseerumata rakud. Neid rakke toidetakse iga päev ja passeeritakse kas ensümaatiliselt või mehaaniliselt iga nelja kuni seitsme päeva tagant. Diferentseerumise tekkimiseks eraldatakse embrüonaalsed tüvirakud abirakkudelt, et moodustuksid embrüonaalsed kehad, kasutades selleks seerumit või muid diferentseerumist soodustavaid meetodeid.
Hiire embrüonaalsete tüvirakkude saamine. Embrüonaalsed tüvirakud eraldati emase doonorlooma varajase embrüo sisemisest rakumassist. Martin Evans ja Matthew Kaufman teatasid meetodist, mis võimaldab hiire embrüo implantatsiooni edasi lükata ja seega kasvatada sisemist rakumassi. Selle protsessi käigus eemaldatakse doonorema munasarjad ja hormoonkeskkonna muutmiseks manustatakse progesterooni, mistõttu embrüod ei kinnitu emakas. Embrüod võetakse ära pärast 4–6 päeva sellises emakasiseses keskkonnas kasvamist ja pannakse kasvama in vitro keskkonda, kuni sisemine rakumass moodustab "munakujulise" struktuuri, mis seejärel muudetakse omakorda üksikrakuliseks ja külvatakse mitomütsiin C-ga (fibroblastide mitoosi vältimiseks) töödeldud fibroblastidele. Üksikrakuliselt kasvatades tekivad klonaalsed rakuliinid. Evans ja Kaufman tõestasid, et sellises rakukultuuris kasvanud hiire rakud suudavad moodustada nii teratoomi kui ka embrüonaalseid kehi, samuti in vitro diferentseeruda, mis kõik kinnitab, et need rakud on pluripotentsed.
Gail Martin eraldas ja kasvatas hiire embrüonaalseid tüvirakke teisiti. Ta eemaldas doonorema embrüod umbes 76 tundi pärast kopulatsiooni ja kasvatas neid öö läbi seerumit sisaldavas söötmes. Kasutades mikrokirurgiat, eraldas ta järgmisel päeval hiire hilise blastotsüsti sisemise rakumassi. Kasvatas seda eraldatud sisemist rakumassi spetsiaalsel söötmel ja mitootiliselt inaktiveeritud fibroblastidel. Nädala pärast ilmusid rakukolooniad, mis kasvasid hästi koekultuuris ja olid pluripotentsete omadustega. Seda näitas rakkude võime moodustada teratoome, diferentseeruda in vitro ja moodustada embrüonaalseid kehi. Martin viitas neile rakkudele kui embrüonaalsetele tüvirakkudele.
Tänapäeval teatakse, et koekultuuris rutiinselt kasutatav seerum sisaldab luu morfogeneetilist valku (BMP) ja toiterakud toodavad leukeemiat inhibeerivat faktorit (LIF), mis on vajalikud hiire embrüonaalsete tüvirakkude diferentseerumise takistamiseks. Need faktorid on äärmiselt olulised hiire embrüonaalsete tüvirakkude efektiivseks kasvatamiseks. Samuti on näidatud, et embrüonaalsete tüvirakkude isoleerimise efektiivsus sõltub hiireliinist. Tänapäeva teadustöös kasutatakse hiire embrüonaalseid tüvirakke transgeensete hiirte, kaasa arvatud knock-out hiirte, tegemiseks.
Inimese embrüonaalsete tüvirakkude loomine on palju keerulisem ja seisab silmitsi eetiliste probleemidega. Seega on paljud teadustöörühmad lisaks inimese embrüonaalsete tüvirakkude uurimisele pühendunud ka indutseeritud pluripotentsete tüvirakkude loomisele.
Võõrpäritolu (ksenogeensete) komponentide probleem tüvirakkude kasvatamisel koekultuuris
Ajakirja Nature Medicine internetiväljaanne avaldas 24. jaanuaril 2005 uurimuse, mis väitis, et inimese embrüonaalsed tüvirakud, mida kasutatakse föderaalseadusega rahastatud teadustöös, on saastunud inimesele mitteomaste molekulidega, mis on tulnud rakkude kasvukeskkonnast. Hiire ja teiste loomade rakkude kasutamine abirakkudena aktiivselt jagunevate rakkude pluripotentsuse säilitamiseks on aga väga levinud meetod. San Diego California Ülikooli teadlaste sõnul seadis embrüonaalsete tüvirakkude kasutamise inimeses ohtu söötmes leiduv inimesele mitteomane siaalhape.
Seevastu väljaande Lancet Medical Journal internetiversioon avaldas 2005. aasta 8. märtsil üksikasjaliku ülevaate, kuidas täielikult raku- ja seerumivabadel tingimustel saadi inimese embrüost uus tüvirakuliin. Need rakud suutsid rohkem kui kuus kuud olla diferentseerumata prolifereeruvas olekus ning moodustada kõige kolme lootelehte rakke nii in vitro tingimustes kui ka teratoomides. Need omadused säilisid edukalt (rohkem kui 30 passeerimisel) ka loodud rakuliinidel.
Doonor-vastuvõtja mittesobivuse vähendamine
Mitmed teadustöörühmad tegelevad embrüonaalsetest tüvirakkudest saadud diferentseerunud rakkude doonor-vastuvõtja mittesobivuse vähendamisega nende siirdamisel patsienti. Üheks võimaluseks oleks patsiendiga geneetiliselt identsete embrüonaalsete tüvirakkude tegemine, kasutades terapeutilist kloonimist.
Alternatiivseks võimaluseks mittekloonitud embrüonaalsete tüvirakkude teraapias on paljude võimalikult erinevate geneetilise taustaga tüvirakuliinide tegemine. Suurima sarnasusega liini kasutamine võimaldaks kohandada ravi vastavalt patsiendile, langetades mittesobivuse riski.
Ohutus: kasvajate tekke riski vähendamine
- Embrüonaalsete tüvirakkude terapeutilisel transplantatsioonil patsienti on suurimaks probleemiks nende võime moodustada kasvajaid, kaasa arvatud teratoome. Sellest tulenevalt peatati ohutuse huvides esimesed embrüonaalsete tüvirakkude kliinilised katsetused, kuigi kasvajaid ei täheldatud.
- Peamine strateegia ohutuse tõstmiseks embrüonaalsete tüvirakkude kasutamises meditsiinis on nende diferentseerimine mõneks kindlaks rakutüübiks (nt närvi-, lihas-, maksarakuks), millega väheneb tüvirakkude tumorigeensus. Pärast diferentseerumist sorteeritakse rakud voolutsütomeetria abil ning tehakse täiendav puhastamine, et saada homogeenne populatsioon.
Esimene kliiniline uuring
I faasi kliinilised katsetused embrüonaalsetest tüvirakkudest saadud oligodendrotsüütide (aju ja seljaaju rakutüüp) transplantatsioonil seljaajuvigastusega isikutele toimusid 2009. aasta 23. jaanuaril. Need said USA toidu- ja ravimiameti heakskiidu ning sellest sai seega maailma esimene inimese embrüonaalsete tüvirakkude inimkatse. Uuringud, mis viisid selle teadusliku saavutuseni, teostasid Hans Keirstead ja tema kolleegid California Ülikoolis Irvine'is.
Nende sooritatud eksperimendis diferentseeriti inimese embrüonaalseid tüvirakke oligodendrotsüütideks ja kasutati transplantatsiooniks. Tulemused näitasid liikumisaktiivsuse taastumist seljaajuvigastusega rottides seitse päeva pärast inimese diferentseeritud tüvirakkude transplantatsiooni. Antud I faasi kliinilises uuringus valiti umbes kaheksa kuni kümme parapleegikut (mõlemapoolselt halvatud), kelle vigastused tekitati vähem kui kaks nädalat enne katsetuste algust, et rakke saaks süstida enne võimaliku armkoe teket. Teadlased rõhutasid, et antud uuringu puhul ei oodatudki patsientide täielikku tervenemist ja kogu liikuvuse taastumist. Uurijad väitsid saadud tulemuste põhjal, et müeliintupe taastumine ja liikuvuse suurenemine on võimalikud.
Esimene teostatud uuring oligi põhiliselt protseduuride ohutuse testimiseks ja oodatud tulemuste korral võib see viia edasiste uuringuteni, kuhu kaasatakse raskemate puuetega inimesi. Uuringud pandi ootele 2009. aasta augustis, kui mitmest käsitletud rotist leiti väike hulk mikroskoopilisi tsüste, kuid keeld tühistati 2010. aasta 30. juulil.
Esimese inimpatsiendi raviks kaasati ja manustati embrüonaalseid tüvirakke Atlantas 2010. aasta oktoobris. Tüvirakuteraapia eestvedaja Geron Corporation arvates kulub tüvirakkudel jagunemiseks mitu kuud ning enne pole võimalik hinnata teraapia edukust või läbikukkumist.
Võimalik meetod uue rakuliini saamiseks
23. augustil 2006 avaldas ajakirja Nature teaduslik internetiväljaanne Robert Lanza kirjutise, mis väitis, et tema meeskond on leidnud võimaluse embrüonaalsete tüvirakkude eemaldamiseks embrüot lõhkumata. Selline tehniline areng võimaldas teadlastel teha tööd uute embrüonaalsete tüvirakkudega, kasutades USA-s avaliku sektori finantseeringuid, samal ajal kui föderaalne rahastamine oli piiratud ja sai kasutada ainult embrüonaalseid tüvirakke, mis olid eraldatud enne 2001. aasta augustit. 2009. aasta märtsis piirang tühistati.
On teada, et viies diferentseerunud rakkudesse kolm geeni (Oct4, Sox2 ja Klf4), saab teha embrüonaalsete tüvirakkude sarnaseid pluripotentseid tüvirakke. Need geenid "reprogrammeerivad" diferentseerunud rakud pluripotentseteks tüvirakkudeks, võimaldades pluripotentsete tüvirakkude teket embrüot kasutamata. Kuna embrüonaalsete tüvirakkude eetilised probleemid on just seotud nende saamisega embrüotest, usutakse, et reprogrammeerimine "indutseeritud pluripotentseteks tüvirakkudeks" võib olla sobivam lahendus. Nii inimese kui ka hiire rakke saab selle meetodiga reprogrammeerida, saades embrüot kasutamata pluripotentseid tüvirakke.
Arvatakse, et patsiendispetsiifilisi embrüonaalseid tüvirakuliine saaks kasutada rakulises asendusravis. Samuti saaks indutseeritud pluripotentsuse metoodika abil arendada embrüonaalsete tüvirakkude liine, mis on saadud erinevate geneetiliste haigustega patsientidelt ja saada seega hindamatu mudel nende haiguste uurimiseks.
Esimene märk sellest, et indutseeritud pluripotentsete rakkude teraapia võib viia uue ravini, oli 6. detsembril 2007 ajakirjas Science avaldatud artikkel, kus Rudolf Jaenischi juhitud uurimisgrupp kasutas seda hiirte sirprakulise aneemia ravis.
16. jaanuaril 2008 teatas California ettevõte Stemagen, et nad lõid täiskasvanult saadud naharakkudest esimese kloonitud inimembrüo. Neist embrüotest oleks võimalik võtta patsiendiga sobivaid embrüonaalseid tüvirakke.
Embrüonaalsete tüvirakkude kasutamine inimese geneetiliste häirete mudelina
Mitmed teadusgrupid on hakanud embrüonaalseid tüvirakke kasutama inimese geneetiliste häirete mudelina. Seda on tehtud rakke geneetiliselt manipuleerides või viimasel ajal ka kasutades pigem implantatsioonieelse geneetilise diagnoosiga (PGD) rakke. Selline lähenemine võib olla väärtuslik erinevate haiguste (nt fragiilse X-i sündroom, tsüstiline fibroos) ja ka nende geneetiliste haiguste uurimises, millel ei ole veel usaldusväärset mudelsüsteemi.