Mitokondriaalne DNA (mtDNA) on mitokondrites asuv DNA (enamik eukarüootse raku DNAst paikneb rakutuumas). Mitokondrid on eukarüootse raku organellid, milles konverteeritakse tsitraaditsükli reaktsioonide kaudu toidus sisalduv keemiliste sidemete energia rakkudele omastatavasse vormi: adenosiintrifosfaat (ATP). mtDNA oli esimene märkimisväärsem sekveneeritud osa inimese genoomist ning seda võib vaadelda kui väikseimat kromosoomi. Suuremal osal liikidest (kaasa arvatud inimesel) pärandub mtDNA ainult emaliini pidi. Mitokondritest pärit DNA järjestus on kindlaks määratud paljudel (kaasa arvatud ka mõnedel väljasurnud) liikidel ning nende järjestuste võrdlemine on fülogeneetika alustalaks. Järjestuste analüüs võimaldab teadlastel hinnata liikidevahelisi evolutsioonilisi kaugusi ja samas lubab ka uurida populatsioonide sugulust, mistõttu on muutunud tähtsaks ka antropoloogias ja bioloogias.
Ajalugu
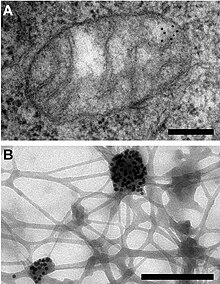
mtDNA avastasid Margit M. K. Nass ja Sylvan Nass 1960. aastatel elektronmikroskoopia abil ning Ellen Haslbrunner, Hans Tuppy ja Gottfried Schatz kõrgelt puhastatud mitokondrite fraktsioonidega biokeemilisi analüüse tehes.
Replikatsioon
mtDNA replikatsiooni viib läbi DNA polümeraas gamma, mis koosneb 140 kDa katalüütilise aktiivsusega alamühikust (kodeerib POLG geen) ja 55 kDa abistavast alamühikust (kodeerib POLG2 geen). Embrüogeneesi ajal on mtDNA replikatsioon alates sügoodi moodustumisest kuni kinnitumata embrüo staadiumini rangelt maha reguleeritud.
Blastotsüsti staadiumis on mtDNA replikatsiooni aktiveerumine iseloomulik trofoblastidele, trofektodermist sissepoole jäävates rakkudes käivitub mtDNA replikatsioon alles siis, kui rakud saavad signaali diferentseeruda spetsiifilisteks rakutüüpideks.
Päritolu
mtDNA ja tuuma DNA arvatakse olevat erineva evolutsioonilise päritoluga. Sümbiogeneesi teooria kohaselt on mtDNA pärit prokarüoodilt, kelle eukarüoodi varajane eellane fagotsüteeris. Hinnanguliselt on igas mitokondris umbes 2–10 mtDNA koopiat. Suuremat osa mitokondris asuvatest valkudest, mis kaasaegsete imetajate rakkudes esinevad (ligikaudu 1500 erinevat tüüpi), kodeerib rakutuuma DNA, kuid mõned neist (kui mitte enamik) arvatakse olevat bakteriaalse päritoluga, mis evolutsiooni käigus on tuuma ümber kolinud.
Mitokondrite pärandumine
Enamikus hulkraksetest organismidest on mtDNA pärit emasorganismidelt. Seda kontrollivate mehhanismide hulgas on lihtne lahjendamine (munarakus on 100 000 – 1 000 000 mtDNA molekuli, spermis kõigest 100–1000 koopiat), spermide mtDNA degradatsioon viljastatud munarakus ning mõnedes organismides ka spermide mtDNA sügooti sisenemise ebaõnnestumine.
Emaliini kaudu pärandumine
Sugulise sigimise puhul päritakse mtDNA tavaliselt ainult emalt. Pärast viljastumist hävitab imetajate munarakk spermide mitokondrid. Lisaks sellele paiknevad mitokondrid tavaliselt spermi sabaosas, mida kasutatakse liikumapaneva jõu tekitamiseks ning tihtipeale ei jõua spermi saba viljastamisel munarakku. Aastal 1999 näidati, et spermide mitokondrid on märgistatud ubikvitiiniga, mis määrab nad arenevas embrüos hukule. Mõned in vitro viljastamise tehnikad, eriti just spermi süstimine ootsüüti, võivad aga seda süsteemi häirida.
Tänu sellele, et mtDNA on matrilineaarne (alternatiivselt uuritakse ka Y-kromosoomi DNAd, mis annab infot patrilineaarsuse kohta), on teadlased võimelised pärandumisliine jälitama ka kaugesse minevikku. Inimesel saavutatakse see (sarnaselt genealoogilise testiga) mtDNA hüpervarieeruvate kontrollregioonide (HVR1 ja HVR2) sekveneerimisega.
HVR1 moodustavad umbes 440 aluspaari, mille järjestus määratakse kindlaks ning võrreldakse seejärel teistelt isikutelt kogutud HVR1 järjestustega. Sagedamini kasutatakse võrdluseks kontrollitud Cambridge'i referentsjärjestust (Cambridge Reference Sequence). Vilà et alia on avaldanud uuringuid, milles näidatakse matrilineaarselt, et koerad põlvnevad hundist. Mitokondriaalse Eeva mõiste põhineb sama tüüpi analüüsil ja üritab avastada inimkonna päritolu, kasutades mineviku rekonstrueerimiseks mtDNA infot.
Kuna mtDNA ei ole tugevalt konserveerunud ja omab kõrget mutatsioonikiirust, sobib see organismidevahelise evolutsioonilise suguluse (fülogeneetika) uurimiseks. Tänu sellele on bioloogid võimelised kindlaks määrama ja võrdlema mtDNA järjestusi erinevate liikide seas ning võrdlusi kasutades koostama uuritud liigi kohta evolutsioonilise puu. mtDNA matrilineaarsus võib osutuda isiku emaliini kohta genealoogiliste uuringute tegemisel väga kasulikuks tööriistaks.
Isaliini kaudu pärandumine
On näidatud, et mõnedel liikidel võivad mitokondrid päranduda ka isaliini pidi, näiteks rannakarbil. Lisaks on patrilineaarselt päritud mitokondreid avastatud putukatel, nagu äädikakärbes, mesilane ja rändrohutirts.
Tõendid kinnitavad, et harvadel juhtudel võivad ka imetajate mitokondrid päranduda isaliini pidi, täpsemalt on juhtumid dokumenteeritud hiirte puhul. Lisaks on seda leitud veel lammastel, kloonitud kariloomadel ning on avastatud ka ühel meessoost isikul.
Struktuur
Enamikus hulkraksetes organismides on mtDNA ringikujuline, kaheahelaline DNA molekul. Inimeste ja tõenäoliselt ka teiste loomade rakkudes on tavaliselt ligikaudu 100 – 10 000 eraldiseisvat mtDNA koopiat (seemne- ja munarakk on erandid). Imetajatel kuulub iga kaheahelalise mtDNA molekuli koosseisu 15 000 – 17 000 aluspaari. mtDNA molekuli kaks ahelat on üksteisest eristatavad nende nukleotiidse koostise poolest, kus guaniinirikast ahelat nimetatakse raskeks ahelaks ja tsütosiinirikast kergeks ahelaks. Raskel ahelal paikneb 28, kergel ahelal 9 geeni, kokku 37. Nendest 37 geenist 13 kodeerivad valke, 22 kodeerivad transportRNAsid (tRNA) ning 2 kodeerivad ribosomaalse RNA suurt ja väikest alamühikut. Selline muster esineb suuremas osas loomadest, kuid on ka juhtumeid, kus üks või rohkem 37 geenist on puudu ja mtDNA molekuli suuruse vahemik on laiem. Seente ja taimede seas esineb veelgi suurem mtDNA geenide varieeruvus, kuid eukarüootide seas paistab olevat kindel põhikomplekt mtDNA geene, mis neis kõigis esineb (välja arvatud need, kellel mitokondrid puuduvad). Mõnedel taimeliikidel esinevad hiiglaslikud mtDNA molekulid (2,5 miljonit aluspaari ühe molekuli kohta), kuid üllatavalt kodeerivad need suured mtDNA molekulid ikkagi sama palju ja sama tüüpi geene kui nende taimeliikide sugulased, kelle mitokondrite genoomid on palju väiksemad. Kurgi mitokondrite genoom koosneb kolmest täielikult või osaliselt autonoomsest tsirkulaarsest kromosoomist (pikkused: 1556, 84 ja 45 kiloaluspaari).
Geenid
NB! mtDNA geenide koosseis varieerub liigiti. Antud lõigus on toodud info inimese mitokondriaalse DNA kohta.
Elektrontransportahel
Mitokondri genoom sisaldab 13-t valku kodeerivat geeni. Nendest paljude geenide produktid kuuluvad elektrontransportahelasse:
| Kategooria | Geenid |
| NADH dehüdrogenaas (kompleks I) | MT-ND1, MT-ND2, MT-ND3, MT-ND4, MT-ND4L, MT-ND5, MT-ND6 |
| Koensüüm Q - tsütokroom c reduktaas/Tsütokroom b (kompleks III) | MT-CYB |
| tsütokroom c oksüdaas (kompleks IV) | MT-CO1, MT-CO2, MT-CO3 |
| ATP süntaas | MT-ATP6, MT-ATP8 |
rRNA
Mitokondri rRNAsid kodeerivad geenid MT-RNR1 (12S) ja MT-RNR2 (16S).
tRNA
tRNAsid kodeerivad järgmised geenid:
| Aminohape | 3-täheline | 1-täheline | MT DNA |
|---|---|---|---|
| Alaniin | Ala | A | MT-TA |
| Arginiin | Arg | R | MT-TR |
| Asparagiin | Asn | N | MT-TN |
| Asparagiinhape | Asp | D | MT-TD |
| Tsüsteiin | Cys | C | MT-TC |
| Glutamiinhape | Glu | E | MT-TE |
| Glutamiin | Gln | Q | MT-TQ |
| Glütsiin | Gly | G | MT-TG |
| Histidiin | His | H | MT-TH |
| Isoleutsiin | Ile | I | MT-TI |
| Leutsiin | Leu | L | MT-TL1, MT-TL2 |
| Lüsiin | Lys | K | MT-TK |
| Metioniin | Met | M | MT-TM |
| Fenüülalaniin | Phe | F | MT-TF |
| Proliin | Pro | P | MT-TP |
| Seriin | Ser | S | MT-TS1, MT-TS2 |
| Treoniin | Thr | T | MT-TT |
| Trüptofaan | Trp | W | MT-TW |
| Türosiin | Tyr | Y | MT-TY |
| Valiin | Val | V | MT-TV |
Mutatsioonid
Tundlikkus
mtDNA on eriti tundlik (just füüsilise läheduse tõttu) hingamisahelas tekkivate reaktiivsete hapnikuühendite suhtes. Kuigi mtDNA on valkude abil kokku pakitud ja omab ka märkimisväärset DNA reparatsioonivõimet, on tema kaitsemehhanismid siiski vähem efektiivsed kui need, mis toimetavad tuuma DNAga, ning arvatavasti annavad seetõttu oma panuse oksüdatiivsete kahjustuste tundlikkusele. mtDNA mutatsioonide tulemuseks võivad olla muutused mõnda valku kodeerivas alas, mis võib avaldada mõju organismi metabolismile ja/või kohasusele.
Geneetilised haigused
mtDNAs toimuvad mutatsioonid võivad põhjustada mitut haigust, näiteks treeningutalumatus või Kearnsi-Sayre’i sündroom (KSS), mille tagajärjel kaotab inimene täielikult südamelihaste, silmade ja skeletilihaste liigutamise funktsiooni. On ka tõendeid, et mtDNAs toimuvad mutatsioonid mõjutavad suuresti vananemisprotsessi ja kujundavad vanusega seotud patoloogilisi seisundeid.
Kasutamine haiguste diagnoosis
Viimasel ajal kasutatakse negatiivse eesnäärme biopsiaga patsientidel eesnäärmevähi avastamiseks mutatsiooni mtDNAs.
Kasutamine identifitseerimises
Inimese mitokondri genoom koosneb 16 569-st aluspaarist, mis esindab kõigest murdosa kogu raku DNAst. Erinevalt tuuma DNAst, mis päritakse mõlemalt vanemalt ja mis rekombinatsiooni käigus ümber korraldatakse, pärandub järglasele tavaliselt samasugune mtDNA nagu vanemal. Kuigi ka mtDNA rekombineerub, teeb ta seda iseenda koopiatega ühe mitokondri piires. Tänu sellele ja faktile, et mtDNA mutatsioonikiirus on suurem kui tuuma DNA-l, on mtDNA võimas töövahend, millega saab uurida põlvnemist naisliine pidi (matrilineaarsus). Seda töövahendit kasutades on teadlastel õnnestunud kindlaks määrata paljude liikide esivanemad sadu põlvkondi tagasi.
Inimese mtDNAd võib kasutada ka isikute tuvastamiseks. Kohtumeditsiini laborid kasutavad aeg-ajalt mtDNAde võrdlemist, et tuvastada inimeste jäänuseid, eriti just vanemate ja tundmatute skelettide tuvastamiseks. Samas pole mtDNA spetsiifiline ainult ühele indiviidile (erinevalt tuuma DNAst) ning seetõttu kombineeritakse seda teiste asitõenditega (antroploogilised asitõendid, pealiskaudsed asitõendid ja nende sarnased), et saavutada tuvastamine. mtDNAd kasutatakse ka tuvastamaks võimalikke vastavusi kadunud isikute ja tuvastamata inimjäänuste vahel. Paljud uurijad usuvad, et mtDNA sobib vanade luujäänuste tuvastamiseks paremini kui tuuma DNA, sest mtDNA molekule on rohkem koopiaid raku kohta ning võimalus, et saadakse kätte kasulik proov, on suurem. Lisaks on veel positiivne ka see, et elava sugulasega võrreldes on võimalik otsitav proov tuvastada ka siis, kui proovi omaniku ja praegu elava sugulase vahele jääb mitu põlvkonda.
Ameerika lindprii Jesse Jamesi maised jäänused identifitseeriti, kasutades võrdlust luudest eraldatud mtDNA ja tema õe lapselapse poja vahel. Sarnaselt tehti kindlaks Venemaa viimase tsarinna Alexandra Feodorovna (Alix of Hesse) ja tema laste isikud mtDNA võrdlustele põhinedes ning leiti sarnasus Edinburghi krahvi prints Philipiga, kelle vanaema oli Victoria of Hesse, Alexandra õde. Nii tuvastati ka keiser Nikolai II maised jäänused, kui tema mtDNAd võrreldi James Carnegie, Fife’i kolmanda krahviga, kelle emapoolne vanavanaema Taani Aleksandra (kuninganna Alexandra) oli Nikolai II ema (tsaarinna Maria Feodorovna) õde.
Väike efektiivse populatsiooni suurus ja suur mutatsioonikiirus (loomades) muudab mtDNA väga kasulikuks indiviidide või gruppide geneetilise suguluse hindamisel liigi piires. Peale selle sobib see hästi ka liikidevahelise suguluse määramiseks, eeldusel, et liigid ei ole liiga kauges suguluses. Et seda saavutada, määravad bioloogid kindlaks mtDNA järjestuse ning seejärel võrdlevad seda mtDNA järjestusega teiselt liigilt või indiviidilt. Võrdlusest saadavaid tulemusi kasutatakse suhete võrgustiku loomiseks, mille alusel hinnatakse evolutsioonilisi suhteid liikide vahel, kellelt proovid koguti.
Sellel lähenemisel on oma piirangud, mis tulenevad mtDNA järjestuse muutuste kiirusest. Loomade puhul on kõrge mutatsioonikiirus kasulik just sama liigi esindajate või lähedases suguluses olevate liikide võrdlemiseks, kelle hulgas on muutuste arvu üsna lihtne kokku lugeda. Kui aga võrrelda erinevamaid liike, siis muutub muutuste arv väga suureks, kuni täpset hinnangut on juba praktiliselt võimatu anda.