Otsing sellest blogist
UUS!!!
Olelusvõitlus ja looduslik valik
Kas olete mõelnud: Miks kaelkirjakul on nii pikk kael? Miks mõned loomad värvuvad talveperioodil valgeks? Mida tähendab väide, et tugevam jä...

kolmapäev, 21. mai 2025
Okazaki fragment
teisipäev, 20. mai 2025
Valgud
Valgud ehk proteiinid (ka valkained) on biopolümeerid, mille monomeerideks on aminohappejäägid. Valgu molekul koosneb paljudest üksteise järele peptiididega seotud aminohapetest, mille järjestuse määrab vastava geeni transkriptsioon. Valkudel on oluline füsioloogiline roll kõikides organismides ja viirustes.

Nimetus
Nimetus "proteiinid" (kreeka keeles protos 'esimene, tähtsaim') pärineb hollandi keemikult Gerardus Johannes Mulderilt, kes võttis selle kasutusele 1839. aastal.
Eestikeelse sõna "valk" lõi Johannes Voldemar Veski sõna "valge" põhjal.
Ülesanded
Valgud on kõige mitmekesisemad makromolekulid elusorganismides. Valkudel on organismis elutähtis roll, sest need osalevad põhimõtteliselt kõikides bioloogilistes protsessides: käituvad katalüsaatoritena, transpordivad ja hoiustavad teisi molekule (näiteks hapnikku), pakuvad mehaanilist tuge ja immuunkaitset, vastutavad rakuliikumise eest, osalevad närviimpulsside ülekandes, kontrollivad kasvu ja rakkude diferentseerumist.
Süstemaatika
Valgud jagunevad lihtvalkudeks ja liitvalkudeks. Liitvalkudes on lisaks lihtvalgulisele komponendile veel mittevalguline täiendav osis ehk prosteeriline rühm. Liitvalgud on näiteks fosfoproteiinid, metalloproteiinid, kromoproteiinid, proteolipiidid, glükoproteiinid jt. Lihtvalkude sekka kuuluvad näiteks albumiinid, globuliinid, histoonid, prolamiinid, gluteliinid, protamiinid ja skleroproteiinid.
Loomseid valke võib jaotada näiteks nende funktsiooni järgi järgmiselt:
- struktuursed valgud
- ensüümvalgud
- transportvalgud
- kaitsevalgud
- kontraktiilsed valgud
- retseptoorsed valgud
- regulatoorsed valgud
- depoovalgud
- eksporditavad valgud
Struktuur ja koostis
Valgud võivad koosneda ühest või mitmest peptiidist. Valgud koosnevad tuhandetest aminohapetest. Polüpeptiididest eristab neid see, et kui polüpeptiidide molekulmass on tavaliselt alla 10 000 daltoni, siis valkudel on see suurem. Molekulmass ei ole seotud bioloogiliselt aktiivsete valkude funktsiooniga. Polüpeptiidide ahelate pikkus on valkudes väga varieeruv, ulatudes sajast paarikümne tuhande aminohappejäägini. Enamik looduslikult esinevatest valkudest sisaldab alla 2000 aminohappejäägi.
Suurim teadaolev inimvalk on südamelihases paiknev titin aatommassiga 3–3,7 megadaltonit (3 000 000 daltonit);
Peptiidid koosnevad aminohappejääkidest. Jääkideks kutsutakse neid seetõttu, et peptiidsideme moodustamisel on aminohape loovutanud vesinikuaatomi aminorühmast ja hüdroksüülrühma karboksüülrühmast, mis sideme tekkimisel eralduvad veemolekulina (dehüdratsioon). Ahela otsas olev vaba α-aminorühmaga jääki nimetatakse aminoterminaalseks (või N-terminaalseks), vaba karboksüülrühmaga jääki karboksüterminaalseks (või C-terminaalseks).
Valgud võivad koosneda nii ühest kui ka mitmest polüpeptiidahelast. Mitmesubühikulised valgud sisaldavad kahte või enamat mittekovalentselt seotud polüpeptiidi, mis võivad olla nii identsed kui ka erinevad. Kui vähemalt kaks ahelat mitmesubühikulises valgus on identsed, on valk oligomeerne ning identsed ühikud, mis koosnevad vähemalt ühest ahelast, on protomeerid. Üksikutel erandlikel valkudel võivad ahelad olla seotud kovalentselt ning sel juhul nimetatakse polüpeptiidahelaid subühikute asemel lihtsalt ahelateks.
Lihtsama struktuuriga valgu aminohappejääkide arvu saab umbkaudselt arvutada jagades molekulmassi 110-ga. Kuigi 20 tavalisema aminohappe keskmine molekulmass on 138 ühikut, esinevad valkudes enamasti väiksemad aminohapped, mille osakaale arvestades on valkude keskmise aminohappe molekulmass 128 ühikut, ning kuna peptiidsideme moodustumisel eraldub veemolekul (M=18 g/mol), taandub keskmine aminohappe molekulmass 110-le.
Valkude aminohappeline koostis on valgule iseloomulik suurus. Samas ei ole valgu täielik hüdrolüüs aminohapeteks valgu aminohappelise koostise määramiseks piisav, sest hüdrolüüsi käigus võivad esineda kõrvalreaktsioonid, näiteks teiseks aminohappeks üleminek või aminohappe täielik lagunemine. Täpse aminohappelise koostise määramiseks kasutatakse vajadusel lisaprotseduure, et hüdrolüüsiga kaasnevaid ebaselgusi lahendada.
Osa valke sisaldavad lisaks aminohapetele ka püsivalt assotsieerunud keemilisi komponente. Selliseid valke kutsutakse konjugeeritud valkudeks ja mitteaminohappelist osa prosteetiliseks rühmaks (lisarühmaks). Konjugeeritud valke liigitatakse prosteetiliste rühmade järgi (näiteks lipoproteiidid sisaldavad lipiide, glükoproteiinid sahhariidrühmi, metalloproteiidid spetsiifilisi metalle).
Valkude struktuuritasemed
- Primaarne struktuur – aminohappeline järjestus. Polüpeptiidahel koosneb regulaarselt korduvast osast – peaahelast ehk selgroost ja muutuvast osast – kõrvalahelatest. Selgrool on suur vesiniksidemete moodustamise potentsiaal, sest iga aminohappejääk sisaldab karbonüülrühma, mis on hea vesiniksideme aktseptor, ning NH-rühma (erandina proliin), mis on hea vesiniksideme doonor. Need rühmad interakteeruvad üksteisega kui ka kõrvalrühmades olevate funktsionaalrühmadega, et konkreetseid struktuure stabiliseerida.
- Mõnedes valkudes on lineaarne polüpeptiidahel ristsidemetega seotud. Kõige tavalisem ristside on disulfiidsild, mis moodustub kahe tsüsteiinijäägi oksüdeerumisel. Tsüsteiinijääkide seondumisel moodustuvat kompleksi nimetatakse tsüstiiniks. Rakuvälistel valkudel on disulfiidisillad tavalised, kuid rakusisestel mitte. Harva esineb ka disulfiidsildade asemel teisi ristsidemeid (näiteks kollageenis).
- Sekundaarne struktuur – aminohappejääkide stabiilne kolmemõõtmeline struktuur (alfaheeliks või beetaleht), ka beetapööre ja oomegasilmus).
- Alfaheeliks – vardasarnane struktuur. Tihedalt pakitud selgroog moodustab varda sisemise osa ning kõrvalahelad on väljapoole suunatud helikaalse struktuuriga. Struktuuri stabiliseerivad peaahela NH- ja CO-rühmade vahelised vesiniksidemed. Iga aminohappejäägi CO-rühm moodustab vesiniksideme NH-rühmaga, mis asub nelja jäägi võrra eespool asuva aminohappejäägi küljes. Üks vesiniksidemetega seotud aminohappepaar moodustab ahelast 1,5 ongströmi (Å) ning keerab ahelat 100⁰ võrra (3,6 aminohappejääki ühe heeliksipöörde kohta).
- Beetaleht – polüpeptiidide ahel on peaaegu täielikult pikenenud, mitte tihedalt kokku pakitud nagu alfaheeliksis. Iga järgneva aminohappejäägi kõrvalahel on võrreldes eelmise jäägiga vastassuunas. Beetaleht moodustub kahe või enama beetaahela seostumisel vesiniksidemetega. Ahelad võivad olla ka vastassuunalised – antiparalleelne ebetaleht, või samasuunalised – paralleelne beetaleht. Enamikul juhtumitel on beetaleheks seostunud 4 või 5 ahelat, aga ahelate arv võib ulatuda kümneni või üle selle. Sellised beetalehed võivad olla ainult antiparalleelsed, ainult paralleelsed või segatüüpi. Beetalehed on suhteliselt lamedad, kuid on veidi väändunud.
- Tertsiaarne struktuur – kogu valgu kolmemõõtmeline struktuur. Polaarsed ja mittepolaarsed aminohappejäägid asuvad enamasti vastavalt struktuuri välispinnal ja sisemuses, sest vesilahustes on valkudel iseloomulik hüdrofoobseid aminohappejääke (näiteks leutsiin, valiin, metioniin, fenüülalaniin) veemolekulidest eraldada. Polaarseteks aminohapeteks on näiteks asparagiinhape, glutamiinhape, lüsiin ja arginiin. Mittepolaarsete osade varjamine vee eest põhineb NH- ja CO-rühmade vaheliste vesiniksidemete ning van der Waalsi interaktsioonide struktuuri stabiliseerivatel omadustel. Valkude kolmedimensioonilisi struktuure uuritakse röntgenkristallograafia ja tuumamagnetresonants-spektroskoopia (NMR või TMR) abil.
- Kvaternaarne struktuur – kahe või enama subühiku ehk alaühiku asend ruumis. Lihtsaim kvaternaarne struktuur on dimeer, mis koosneb kahest identsest subühikust (SU).
Christian Anfinsen kirjeldas 1950ndatel aminohappejärjestuse ja valgukonformatsiooni vahelist seost ensüümi ribonukleaas põhjal.
Rakkudes takistavad valgul vale konformatsiooni võtmist erilised valgud – šaperonid (tugivalgud).
Funktsioonid
Valgu funktsioon on otseselt seotud tema kolmemõõtmelise struktuuriga. Seega kujutab valk endast ülekannet ühedimensioonilisest järjestusest kolmedimensiooniliste molekulideni, mis on võimelised mitmekülgseks aktiivsuseks. Kui valk kaotab struktuurimuutuste järel oma ensümaatilise aktiivsuse, on tegemist valgu denatureerumisega.
Paljude valkude funktsiooniks on teiste molekulide sidumine. Seotavat molekuli kutsutakse ligandiks. Ligandiks võib olla igat tüüpi molekul, ka valk. Ligandide mööduv seondumine on elusorganismis äärmiselt oluline, sest lubab organismil reageerida keskkonnamuutuste ja metabolismiseisunditele kiiresti ja pöörduvalt. Ligandi seostumise kohta valgus kutsutakse sidumiskohaks, mis on ligandi suuruse, kuju, laengu ja hüdrofiilsete või -foobsete omadustega komplementaarne. Ligandi seostumine on spetsiifiline, sest iga sidumiskoht saab interakteeruda vaid ühe või mõne ligandiga. See on väga tähtis elusorganismide kõrge organiseerituse säilitamiseks.
Ensüümid
 Valkude struktuur on liikuv. Konformatsioonimuutused võivad olla alates aminohappejääkide molekulaarsetest vibratsioonidest kuni mitmenanomeetriliste muutusteni segmentide liikumisel. Spetsiifilised konformatsioonilised muutused on sageli valgu funktsiooni jaoks vajalikud. Valgu ja ligandi seondumisega kaasneb enamasti ka konformatsioonimuutus, mis teeb sidumiskoha ligandi jaoks komplementaarsemaks, mis viib selle tugevama seondumiseni. Multisubühikulistes valkudes mõjutab ühe subühiku konformatsioonimuutus ka teiste subühikute kuju. Ensüümid on erilise funktsiooniga valgud, sest seondavad ja muudavad keemiliselt teisi molekule – katalüüsivad reaktsioone. Ensüümidega seonduvaid molekule kutsutakse ligandide asemel substraadiks ning ligandi seostumise kohta kutsutakse aktiivtsentriks. Ensümaatiline katalüüs on elusorganismidele hädavajalik, sest bioloogiliselt vajalikes tingimustes on mittekatalüseeritud reaktsioonid enamasti aeglased, sest enamik bioloogilisi molekule on rakkudes oleva neutraalse pH, mõõduka temperatuuri juures ja veekeskkonnas üsna stabiilsed. Lisaks sellele ei ole mitmete vajalike biokeemiliste reaktsioonide toimumine soodustatud või on ebatõenäoline.
Valkude struktuur on liikuv. Konformatsioonimuutused võivad olla alates aminohappejääkide molekulaarsetest vibratsioonidest kuni mitmenanomeetriliste muutusteni segmentide liikumisel. Spetsiifilised konformatsioonilised muutused on sageli valgu funktsiooni jaoks vajalikud. Valgu ja ligandi seondumisega kaasneb enamasti ka konformatsioonimuutus, mis teeb sidumiskoha ligandi jaoks komplementaarsemaks, mis viib selle tugevama seondumiseni. Multisubühikulistes valkudes mõjutab ühe subühiku konformatsioonimuutus ka teiste subühikute kuju. Ensüümid on erilise funktsiooniga valgud, sest seondavad ja muudavad keemiliselt teisi molekule – katalüüsivad reaktsioone. Ensüümidega seonduvaid molekule kutsutakse ligandide asemel substraadiks ning ligandi seostumise kohta kutsutakse aktiivtsentriks. Ensümaatiline katalüüs on elusorganismidele hädavajalik, sest bioloogiliselt vajalikes tingimustes on mittekatalüseeritud reaktsioonid enamasti aeglased, sest enamik bioloogilisi molekule on rakkudes oleva neutraalse pH, mõõduka temperatuuri juures ja veekeskkonnas üsna stabiilsed. Lisaks sellele ei ole mitmete vajalike biokeemiliste reaktsioonide toimumine soodustatud või on ebatõenäoline.
Ensüümid on äärmisel efektiivsed katalüsaatorid. Nad muudavad madalamaks reaktsiooni aktivatsioonienergia ning suurendavad sellega reaktsiooni kiirust (106 pealt 1017-ni). Ensüümkatalüüsitud reaktsioonidele on iseloomulikuks substraadi ja ensüümi vahel tekkiv kompleks. Ensüüm ei mõjuta reaktsiooni tasakaalu. Seostumisenergiat saab kasutada substraadi entroopia madaldamiseks või ensüümis konformatsioonilise muutuse esilekutsumiseks. Seostumisenergia seletab ka ensüümide väga suure täpsuse substraatide suhtes.
Oluline osa ensümaatilise kiiruse suurendamiseks vajalikust energiast saadakse substraadi ja ensüümi vahel olevatest nõrkadest interaktsioonidest (vesiniksidemed ning hübrofoobsed ja ioonilised interaktsioonid). Ensüümi sidumiskoht on struktureeritud nii, et mõned nendest nõrkadest interaktsioonidest esinevad eelistatult reaktsiooni üleminekuolekutes, et neid stabiliseerida. Paljude interaktsioonide vajalikkus põhjustab ka selle, et ensüümid on suurte mõõtmetega.
Teised ensüümide kasutatavad katalüütilised mehhanismid on näiteks happe-aluse katalüüs, kovalentne katalüüs ja metalliiooni katalüüs. Katalüüs sisaldab mööduvaid kovalentseid interaktsioone substraadi ja ensüümi vahel või funktsionaalsete rühmade üleminekuid ensüümile või selle küljest.
Valgusüntees
 Valgusüntees on mitmeastmeline protsess, milles rakud taastoodavad valke. See algab aminohappe sünteesist ja tuumast pärineva DNA transkriptsioonist mRNA-ks, mis on hiljem translatsiooni alginformatsiooniks ning määrab valgu aminohappelise järjestuse. Translatsiooni viivad läbi ribosoomid, mis koosnevad rRNAst ja valkudest. Selle käigus kinnitub ribosoom mRNA otsale ning liigub piki ahelat edasi, püüdes aminohapetega seondunud tRNA-sid ja lubades mRNA koodonitel paarduda sobivate tRNA antikoodonitega. tRNA küljes ribosoomi kantud aminohapejäägid liidetakse kokku peptiidsidemete abil ning vabad tRNA-d vabastatakse protsessist. Pärast võib aset leida veel valgu keemiline modifitseerimine, mida nimetatakse posttranslatsiooniliseks modifikatsiooniks, ja valgu voltumine.
Valgusüntees on mitmeastmeline protsess, milles rakud taastoodavad valke. See algab aminohappe sünteesist ja tuumast pärineva DNA transkriptsioonist mRNA-ks, mis on hiljem translatsiooni alginformatsiooniks ning määrab valgu aminohappelise järjestuse. Translatsiooni viivad läbi ribosoomid, mis koosnevad rRNAst ja valkudest. Selle käigus kinnitub ribosoom mRNA otsale ning liigub piki ahelat edasi, püüdes aminohapetega seondunud tRNA-sid ja lubades mRNA koodonitel paarduda sobivate tRNA antikoodonitega. tRNA küljes ribosoomi kantud aminohapejäägid liidetakse kokku peptiidsidemete abil ning vabad tRNA-d vabastatakse protsessist. Pärast võib aset leida veel valgu keemiline modifitseerimine, mida nimetatakse posttranslatsiooniliseks modifikatsiooniks, ja valgu voltumine.
Prokarüootide ja eukarüootide valgusüntees on erinev. Prokarüootides toimub translatsioon tsütoplasmas, eukarüootide puhul endoplasmaatilises retiikulumis.
Lühemaid valgujärjestusi suudetakse tänapäeval edukalt sünteesida ka keemiliste meetodite abil. Seejuures on sel viisil võimalik mittekanooniliste aminohapete liitmine valgujärjestustesse.
Valkude eraldamise meetodid

 Konkreetsete valkude eraldamiseks valkude segust on erinevaid meetodeid:
Konkreetsete valkude eraldamiseks valkude segust on erinevaid meetodeid:
- väljasoolamine – eri valgud sadestuvad erineva soolakontsentratsiooni juures;
- dialüüs – eraldamine läbi poolläbilaskva membraani;
- geelfiltratsioonkromatograafia – suuremate ja väiksemate molekulide erinev liikuvus läbi geeli;
- ioonivahetuskromatograafia – laenguga valkude seondumine kolonni;
- afiinsuskromatograafia – valkude afiinsus spetsiifiliste keemiliste rühmade suhtes;
- kõrgefektiivne vedelikkromatograafia (kõrgsurvevedelikkromatograafia).
esmaspäev, 19. mai 2025
NAD (Nikotiinamiid adeniin dinukleotiid )
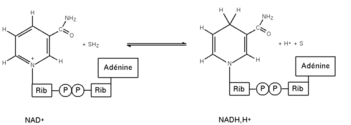
Nikotiinamiid adeniin dinukleotiid ehk NAD on kõigis elusates rakkudes levinud koensüüm. See esineb kahes vormis, millest redutseeritud on NADH ja oksüdeeritud NAD⁺.
Seda ühendit nimetatakse dinukleotiidiks, sest see on moodustatud kahest nukleotiidist, mis on omavahel ühendatud fosfaatgruppide vahendusel. Ühe nukleotiidi koostisse kuulub adeniin ja teise koostisse nikotiinamiid. Nikotiinamiid on ühtlasi selle elektronkandja reaktiivseks osaks ja see on tuntud ka kui B3-vitamiin ehk niatsiin.
NAD⁺ osaleb redoksreaktsioonides, kus ta oksüdeerijana seob kaks elektroni ja vesinikaatomi, ja tekib redutseeritud vorm NADH. NADH on seega aktiveeritud kandja, mis kannab toitainete oksüdeerimisel elektrone.
NAD⁺ on vahelüli toitainete oksüdeerumisel, mille käigus võtab suure potentsiaaliga elektronid lõpuks vastu O2. Aktiveeritud kandjatel on suurem elektronafiinsus kui süsinikühenditel, kuid väiksem afiinsus kui O2-l. Aktiveeritud elektronid liiguvad väiksema afiinsusega kandja juurest suurema afiinusega kandja juurde, selline elektronide liikumine tagab nende edasikandumise O2-le läbi elektronide transpordiahela. Hoolimata sellest on NADH väga stabiilne, mis on väga oluline bioloogilisest seisukohast vaadatuna, sest võimaldab reguleerida ensüümidega vaba energia vallandumist.
Funktsioon biokeemilistes protsessides
Glükolüüs
Glükolüüsi teises etapis, kus kolmesüsinikulised ühendid muundatakse püruvaadiks, kasutatakse taandajana NAD⁺-i. Redoksreaktsiooni käigus muudetakse glütseeraldehüüd-3-fosfaat ehk GAP 1,3-bifosfoglütseraadiks, mida tehakse glütseeraldehüüd-3-fosfaadi dehüdrogenaasi abil. Dehüdrogenaasid kasutavad tavaliselt katalüüsil NAD⁺-i või NADH-i, olenevalt sellest kas H-aatomit on vaja siduda või kanda üle aktseptormolekulile.
Selleks, et glükolüüs kestaks edasi, on vaja taastoota NAD⁺-i. Seda tehakse püruvaadi metaboliseerimise käigus. Glükoosist tekib püruvaat, mis võib muunduda edasi kolmel viisil:
- laktaadiks,
- etanooliks,
- CO2-ks ja veeks.
Fermentatsioonid ehk käärimised on protsessid, mis toimuvad anaeroobsetes tingimustes ja mille käigus tekib ATP. Fermentatsioonid on üks viis, kuidas oksüdeerida NADH-i ja taastoota NAD⁺-i. Alkoholkäärimise käigus tekib NAD⁺ atseetaldehüüdi muundumisel etanooliks. Piimhappekäärimises tekib NAD⁺ püruvaadi muundumisel laktaadiks. Mõlemaid protsesse viib läbi rakusisene ensüüm dehüdrogenaas, mis viitab NADH-i ja NAD⁺-i kasutamisele reaktsioonis.
Glükoneogenees
NAD⁺-i kasutatakse ka glükoneogeneesis, protsessis, kus sünteesitakse glükoosi püruvaadist. NADH-d kasutatakse glütseeraldehüüd-3-fosfaadi tekkimiseks. Reaktsioon on glükolüüsiga ühine.
Tsitraaditsükkel
Tsitraaditsüklit ettevalmistavates reaktsioonides tekib püruvaadist püruvaadi dehüdrogenaasi kompleksis atsetüülkoensüüm-A (atsetüül-CoA). Atsetüül-CoA-i tekkeks on vaja koensüüm-A-d ja NAD⁺-i. Et püruvaadi dehüdrogenaasi kompleks saaks läbi viia ka järgmist reaktsiooni, tuleb taastada lipoamiidi algne vorm. Lipoamiid on vajalik, et püruvaadist tekiks atsetüül-CoA. Taastamisprotsessis on samuti vaja NAD⁺-i.
Tsitraaditsüklis ei saada palju adenosiintrifosfaati ehk ATP-d, kuid kasutatakse NAD⁺-i kolm korda. See tähendab, et tsitraadist eraldatud elektronid seotakse ja tekib kolm korda NADH-i, mida kasutatakse ATP tootmisel. Tsitraaditsüklis liiguvad elektronid läbi membraani, kasutades selleks valke, ning liikumisel tekib prootongradient, mis aitab ADP-st toota ATP-d. Tsitraaditsükkel koosneb kahest osast, kus esimeses NAD⁺-i kandjaid kasutatakse isotsitraadi muundamisel a-ketoglutaraadiks ja viimase muundamisel suktsinüül-CoA-ks. Teises osas kasutatakse NAD⁺-i malaadi muundamisel uuesti oksaalatsetaadiks.
Tsitraaditsükli kataboolne põhifunktsioon on kõrge energiaga elektronide saamine NADH- ja FADH2-na. Tsitraaditsüklis moodustunud NADH ja FADH2 oksüdeeritakse elektronide transpordiahela abil, mille tulemusena saadakse lõpus 2,5 ATP-i molekuli NADH-i kohta ja 1,5 ATP-i molekuli FADH2-i kohta.
Tsitraaditsüklit reguleeritakse NADH-i abil. Kui rakus on NADH-i palju, siis inhibeerub isotsitraadi dehüdrogenaas ja samuti a-ketoglutaraadi dehüdrogenaas, sellega on kontrollitud tsitraaditsükli kiirus. Oluline on ka see, et tsitraaditsüklis on ensüüme, mis vajavad NAD⁺-i või FAD-i. "Need ensüümid töötavad tingimustes, kus raku energialaeng on madal, sest ainult siis on NAD⁺ ja FAD saadaval".
Glükosülaaditsükkel
Glükosülaaditsükli abil saavad taimed ja bakterid muundada rasvu süsivesikuteks. Glükosülaaditsükli reaktsioonid klapivad tsitraaditsükli omaga, kuid puuduvad dekarboksüülimisreaksioonid. Seega kasutatakse siin tsüklis ühte NAD⁺-molekuli koos malaadi dehüdrogenaasiga, et saada malaadist oksaalatsetaat.
Elektronide transpordiahel
Elektronide transpordiahel on membraanis asuvate valkude kompleks, mille kaudu liiguvad NADH-lt saadud elektronid. Valgukomplekse on kolm. Kui elektronid liiguvad transpordiahelas, tekitab see prootongradiendi, mida saab kasutada ATP sünteesiks ja metaboliitide transpordiks.
"Oksüdatiivse fosforüülimise liikumapanevaks jõuks on NADH-i elektronide ülekandevõime O2 suhtes". Elektronide ülekanne NADH-lt O2-le on eksergooniline protsess.
Elektronide transpordiahelas kanduvad elektronid NADH-lt üle O2-le mitmete kandjate abil, mis kokku moodustavad kindla rea. Rida on seatud nii, et elektronid liiguvad alati kandjate poole, millel on suurem elektronide afiinsus. NADH-i elektronide esimesena läbitav valgukompleks on NADH-Q oksüdoreduktaas, mis on väga suur valgukompleks ja transpordib prootoneid maatriksist välja. Hingamisahela ülesanne seisneb NAD⁺-i taastootmises, milleks ta peab sisenema mitokondrisse, kuid mitokondri sisemembraanist ei pääse läbi NAD⁺ ega NADH. Seega viiakse NADH-i elektronid mitokondrisse süstiku abil.[1]
Glükoosi täielikul oksüdeerimisel tekib 18 NADH-i molekuli. Oksüdatiivset fosforüleerimist saab NADH-i abil pidurdada kahel etapil:
- elektronide transpordiahela pidurdamine
- elektronide transpordi eraldamine ATP sünteesist
Oksüdatiivse fosforüleerimise pidurdamist tekitavad paljud mürgid, mis on surmavad või tugevalt kahjustavad.
Rasvhapete lagundamine
Rasvhapete oksüdeerimisel tekib NADH. Palmitoüül-CoA lagundamiseks läheb vaja 7 NAD+-molekuli, sest igas reaktsioonitsüklis eraldub üks NADH-molekul, aga reaktsioonitsüklit peab läbi viima seitse korda.
Rasvhapete lagunemisel tekib peale atsetüül-CoA ka ketokehasid. Ketokehade kasutamisel energiaallikana tekib NADH.
Aminohapete süntees
NADH-i kasutatakse asendavate aminohapete sünteesil (aminohapped, mida inimene suudab ise sünteesida).
NAD⁺ ja vananemine
Rakud kasutavad NAD⁺-i sirtuiini aktiveerimiseks. Sirtuiin on valk, mis kiirendab ainevahetust, vähendab rakustressi ja pikendab raku eluiga. Sirtuiinididel on oluline roll telomeeride pikkuse säilitamisel ning telomeeride pikkust on seostatud pika elueaga.
Mida vanemaks inimene saab, seda madalamaks muutub NAD⁺-i tase kehas. Põhjuseks on CD-38, mis hävitavad NAD⁺-i kehale mittekahjulikule tasemele. Tegelikult aitab NAD⁺-i hävitamine reguleerida unetsüklit ja toitumist. NAD⁺-rikaste toidulisandite manustamisel on võimalik vananemisprotsessi edasi lükata.
NAD⁺ ja haigused
Kliiniline huvi NAD⁺-i vastu tekkis siis, kui avastati, et NAD⁺ või selle aktiveeritud sirtuiinid toetavad mitokondri funktsioone. NAD⁺-i abil saab ravida haigusi, mis on mitokondriaalse tekkega, varieerudes geneetilistest mitokondriaalsetest haigustest kuni vähini, ning vananemisega seotud haigusi, nii metaboolseid kui ka närvisüsteemi haigusi.
reede, 16. mai 2025
Kometabolism
Kometabolism on raskesti muundatavate ühendite kasutamine mitme eritasemelise organismi järjestikuses talitluses.
Tavaliselt on ettevalmistavateks muundajateks mikroobid, kelle elutegevuse tulemusena muutuvad raskesti muundatavad ühendid kasutatavaks teistele organismidele (nt taimedele ja loomadele).
Kometabolismi protsessid toimuvad ka inimese seedekulglas.
neljapäev, 15. mai 2025
Anabolism
Anabolism ehk assimilatsioon on organismis aset leidvate ainevahetuslike protsesside kogum, kus lihtsamatest keemilistest ühenditest sünteesitakse keerulisemad ühendid. Protsessi käigus vajatakse energiat ja ainet. Sõna "anabolism" tuleb kreeka keelest: ἁνά ana "ülespoole" and βάλλειν ballein "viskama".
Anabolismi vastandprotsess on katabolism. Katabolismi käigus lõhustatakse suured molekulid väiksemateks osadeks ja neid omakorda kasutatakse hingamisel. Paljusid anaboolseid protsesse varustab energiaga ATP (adenosiintrifosfaat).
Laias laastus võib öelda, et anaboolsete protsesside käigus moodustuvad rakkude diferentseerumise ja suurenemise tõttu koed ja elundid, ning mis omakorda viib ka organismi kehamõõtmete suurenemisele.
Anaboolsetest protsessidest on ökoloogilist aspekti rõhutades tähtsaim fotosüntees.
kolmapäev, 14. mai 2025
Katabolism
Katabolism ehk dissimilatsioon ehk lagundav ainevahetus (kreeka katabolē 'allaviskamine', sõnadest κατά kata, "allapoole" ja βάλλειν ballein, "viskama") on organismis hapniku kaasabil toimuv keemiline protsess, ainevahetuse osa, milles keerulisematest ainetest tekivad lihtsamad ja milles vabaneb energiat.
Katabolism on polümeeride biolagundamine ensüümide toimel monomeerideni (näiteks tselluloos glükoosini) või lihtsate orgaaniliste aineteni (glükoosi lagundamine CO2 ja H2O-ni).
Dissimilatsiooni moodustavad organismi kõik lagundamisprotsessid. Toiduga saadavad või organismis sünteesitud orgaanilised ühendid lõhustatakse ensüümide abil järk-järgult lihtsama ehitusega molekulideks. Selles protsessis võime eristada biopolümeeride hüdrolüüsi (nt. tärklise lagundamist glükoosi molekulideks) ja sellele järgnevat monomeeride (nt. glükoosi) oksüdatsiooni. Enamiku dissimilatsiooni protsessidega kaasneb energia vabanemine. See talletatakse energiarikastesse ehk makroergilistesse ühenditesse umbes 40% kasuteguriga. Üheks peamiseks makroergiliseks ühendiks on ATP (adenosiintrifosfaat). Viimasel on oluline roll ka assimilatsiooni protsessides. Dissimilatsioonist ja assimilatsioonist koosneb organismi metabolism.
teisipäev, 13. mai 2025
Metabolism
Metabolism (kreeka keeles μεταβολή metabolē 'muutus') ehk ainevahetus tähendab organismis aset leidvaid sünteesi- ja lagundamisprotsesse. Metabolism on kõikide elusorganismide rakkudes toimuvate keemiliste reaktsioonide, mille osalusel toimuvad elusrakkudes keemilise energia protsessid, tulem. Terves organismis on sünteesi- ja lagundamisprotsessid omavahel tasakaalus. Oluline osalejamolekul metabolismis on vesi. Metabolism hõlmab biokeemilisi reaktsioone näiteks selliste orgaaniliste molekulidega nagu:
Ainevahetuse moodustavad kaks vastandprotsessi – katabolism ja anabolism.
esmaspäev, 12. mai 2025
Ateroskleroos
Ateroskleroosiks ehk arterite putrumuskõvastu(mu)seks ehk arterilubjastuseks (ladina keeles atherosclerosis) on osadel inimestel ja teistel selgroogsetel loomadel esineda võiv krooniline, kuni aastakümneid asümptomaatiliselt arenev, südame-veresoonkonna põletikuline haiguslik seisund. Ateroskleroosi iseloomustab aterosklerootiliste muutuste (naast) tekkimine arteriseinte sise- ja keskkestale kuhjuvate kolesterooliladestuste näol.
Ateroskleroosi tekke põhjuseid veel ei teata, kuid oletatavatest peetakse olulisemaks vanadust, loomarasvarohket toitu, perekondlikke rasvaainevahetushaigusi, soonte kroonilisi põletikulisi seisundeid ja ka autoimmuunhaigust.
Ateroskleroos on arenenud maades surmapõhjustest esikohal.
Südame isheemiatõbi on üks ateroskleroosi avaldumisvorm.
Ateroskleroos on arterioskleroosi üks vormidest. See avaldub alguses silelihaskoe rakkude hüperplaasia või hüpertroofiana ja maatriks-proteiinide (ingl matrix-proteins) kuhjumisena suurte ja keskmiste arterite intimas ehk sisekestas (ühe endoteeliraku paksune kiht). Sisekesta tekkivad kaltsiumist, rasvainest (nagu näiteks kolesterool ja triglütseriidid), fibriinist, lihasrakkudest ja sidekoest paksendid. Paksendid võivad hiljem sidekoestuda ja lubjastuda ning selle tagajärjel võivad arterid aheneda ja rabedaks muutuda ning vereringlust takistada ja see omakorda võib vererõhku tõsta.
Ateroskleroos kahjustab kõige sagedamini aorti, pärgartereid, peaaju veresooni ja seda peetakse müokardi infarktide ja insultide levinuimaks põhjustajaks. Lisaks võivad patoloogiliseks peetavad muutused toimuda ka peensoolekinnisti ja kõhunäärme veresoonkonnas.
William C. Robertsi arvates on ateroskleroos valdavalt herbivoorsete loomade haiguslik seisund, kuna koertel, kassidel, tiigritel ja lõvidel pole õnnestunud ateroskleroosi indutseerida. Kilpnäärme eemaldamise järel tekivad ka neil arterites aterosklerootilised muutused.
Inimesel
Riskitegurid
Ateroskleroosi levinumad ja tõenäolised riskitegurid liigitatakse kaheks:
- mittemõjutatavad riskitegurid – meessugu, päritolu, vanus, perekondlikud südamehaigused, perekondlikud lipiidide ainevahetuse häired;
- mõjutatavad riskitegurid – hüperkolesteroleemia, arteriaalne hüpertensioon, suitsetamine, suhkurtõbi.
Psoriaasil ja ateroskleroosil on ühiseid riskitegureid ja tõestatult ka sarnaste immunoloogiliste mehhanismide esinemine, näiteks T-abistajarakkude tasakaalu häire ja tsütokiinide profiili muutused.
Vähem oluliseks või ebaselgeks peetakse vitamiinivaegust, liigsöömist (rasvumine), vähest liikuvust, postmenopausaalset östrogeenide defitsiiti, süsivesikurikast dieeti, kolesteroolirikast ning puu-, juur- ja teraviljavaest toitu, Chlamydia pneumonia infektsiooni ja ka häireid lümfoid(-immuun)süsteemi töös.
Ateroskleroosi riskiteguriteks peetakse epidemioloogiliste uuringute alusel madalat HDL-kolesterooli taset.
Ateroskleroosi perekondlikeks riskiteguriteks on
- kaasasündinud anormaalne apoA metabolism
- kaasasündinud apoB sünteesi täielik puudumine
- kaasasündinud apoE isovormide disbalanss või ehitusdefektid
- kaasasündinud häired LDL-retseptorite sünteesis, talitluses, "valmimises" (retseptorite täielik puudumine või ka väga madal afiinsus jt)
- perekondlik hüperkolesteroleemia
- kaasasündinud LPL ja/või tema aktivaatori apoC-2 puudus/osaline defitsiit
- rasvaainevahetushaigus, millest tingituna kuhjub kolesterool vereringes (arterite seintes) ja arter hakkab ahenema.
Tekkemehhanismi kirjeldus
Kõrgenenud LDL-kolesterooli tase võib organismis, ebasoodsates tingimustes (arteri sisemine kiht on eelnevalt kahjustada saanud) arterite seinte sisekihi ehk endoteeli alla ladestuda, kus hakkavad moodustuma rasvajutid. Lipiidseid vööte ja plekke võib kohata juba 6-kuuste väikelaste ja 50% 10-aastate koolilaste mõningate veresoonte siseseintel. Rasvajuttide levik kutsub omakorda esile monotsüütide ja T-lümfotsüütide kogunemise ja nende aktiveerumise nimetatud piirkonnas. Aktiveerunud monotsüüdid muutuvad makrofaagideks ja hakkavad komplekteerima tsütokiine, vabu radikaale ja proteolüütilisi ensüüme. Lisaks eeltooduile, esinevad ateroskleroosi 'naastudes' autoantigeenid, autoantikehad, B-lümfotsüüdid, loomulikud tappurrakud, koesobivusantigeenid, jne. HDL-kolesterooli osakesed aga vabastavad makrofaagidest taas kolesterooli ja juhivad vereringesse.
Põhjustajad
Arterite põletikulisi protsesse võivad põhjustada ka mitmed bakterid ja viirused (näiteks Herpes simplex'i viirus). Mitmed epidemioloogilised uuringud seostavad ateroskleroosi teket ka bakteri Helicobacter pylori infektsiooniga.
Liigid
Aterosklerootilisi muutusi võib esineda mitmesugustes elundites ja kudedes, nii südame, peaaju, käte, jalgade ja neerude arterites põhjustades vastavas elundis kliinilisi nähtusid:
- südame pärgarteri kahjustuse korral võib välja areneda südame pärgarterite ateroskleroos;
- ajuarteri kahjustuse korral peaaju arterite ateroskleroos (isheemiatõbi);
- neeruarterite kahjustuse korral võib hakata arenema hüpertooniatõbi ja neeruarterite ateroskleroos;
- niude- või reie veresoonte kahjustuse korral võib tekkida jäsemearterite ateroskleroos.
Klassifikatsioon
Aterosklerootilisi muutusi klassifitseeritakse käesoleval ajal naastude ulatuse ja tugevuse ning 'puhkemise' ja muude näitajate alusel tüüpideks I–VI.
Aterosklerootiliste kahjustuse järgud
- prelipiidne järk;
- lipoidoosijärk;
- fibroosijärk;
- ateromatoosijärk;
- kaltsinoosijärk;
- tüsistuste järk.
Aterosklerootilises veresoones võib üheaegselt esineda mitmele järgule omaseid muutusi.
Ravi
Kuna ateroskleroosi täpseid tekkemehhanisme ja päritolu ei tunta siis ei teata ka ravi selle progresseeruva seisundi ja selle sümptomaatika vastu. Ateroskleroos võib sõltuvalt veresoone sulgumise kohast arteris, põhjustada kas insulti, gangreeni, akuutset müokardi infarkti või seniilse dementsuse ilminguid. Ateroskleroosi diagnoosi kinnitamise korral võivad arstid aterosklerootilisele patsiendile määrata elukestva tabletiravi statiinidega.
Koos tavapäraste ravimitega võidakse aterosklerootilisele patsiendile soovitada ka eeldatavalt kasuliku toimega toidulisandeid nagu küüslauk, E-vitamiin, viirpuu (viljad, lehed, õied), koensüüm Q10 (CoQ10) (ubikinoonid), oomega-3-rasvhapped (kalamaksaõli), fütosteroolid, ja kaltsiumi, magneesiumi, kaaliumi, B-vitamiine, C-vitamiini sisaldavaid vitamiinipreparaate.
Ka India nonipuu lehtedes (Morindae citrifoliae folium) leiduva prokseroniiniga on seostatud ateroskleroosi vähenemist.
Rahvameditsiinis
Rahvameditsiinis on hariliku õlipuu lehti kasutatud kui ateroskleroosi leevendavat vahendit.
Loommudelid
Biomeditsiini uuringutes kasutatakse ateroskleroosi-loommudeli (biotest) loomadena tihti jäneseid. kuid katsete tulemused on varieeruvad, kuna alati ei õnnestu neil loomadel ateroskleroosi esile kutsuda.
Ajaloolist
- 1755 pakkus Albrecht von Haller välja termini atheroma kirjeldamaks degeneratiivseid muutusi arterite seintes.
- 1815 avaldas Briti kirurg teose "Treatise on the Diseases of Arteries and Veins", kus väitis, et arterite aterosklerootiliste muutuste põhjuseks on põletik.
- 1858. aastal kirjeldas Rudolf Virchow teoses "Die Cellularpathologie in ihrer Begründung auf physiologische und pathologische Gewebelehre" põletikulisi muutusi aterosklerootiliste soonte seintes.
- 1908. aastal avaldas Ignatowski, Aleksander C. uurimuse "Influence of animal food on the organism of rabbits", mille käigus tekitati jänestel loomse toidu söötmisega eksperimentaalne ateroskleroos, tõestamaks seisundi seotust toiduga.
reede, 9. mai 2025
Bioakulumatsioon
Bioakumulatsioon on nähtus, kus organismi kogunevad toksilised ained suurema kiirusega kui need ainevahetuse käigus organismist eritatakse.
Seega, mida pikem on mingi aine bioloogiline poolestusaeg, seda suurem on kroonilise mürgistuse oht.
Inimorganismi võivad bioakumuleeruda nt pliiühendid, mis mingi kontsentratsiooni juures hakkavad negatiivselt mõjutama inimorganismi, ja mille lõpptulemusena inimene võib surra. Bioakumuleeruda võivad ka dioksiinid.
Bioakumulatsioon võib ilmneda ka pideva reostusallika olemasolul ainete puhul, mille püsiva seondumise võime organismi kudedega on väike. Näiteks võivad bensiinitankla lekkivad mahutid põhjustada põhjavee kaudu nii joogivees, toidus kui ka selles piirkonnas elavate inimeste organismides püsiva MTBE (bensiinilisandina kasutatava antidetonaatori) sisalduse ning tekitada mitmesuguseid ainevahetuse ning närvisüsteemi talitluse häireid.
Sõnavara
Ehkki sageli mõistetakse termineid "bioakumulatsioon" ja "biokontsentratsioon" samatähenduslikena, on viimast on defineeritud ka kui veekeskkonnas elava organismi metabolismi käigus veest võetavate ainete suurem kogus kui eritatavate ainete kogus (Landrum & Fisher, 1999).
neljapäev, 8. mai 2025
Biolagunemine
Bioloogiline lagunemine ehk biolagunemine ehk biodegradatsioon on orgaaniliste ainete muundumine lihtsateks anorgaanilisteks aineteks (CO2, H2O, NH3) mikroorganismide toimel. Erinevad orgaanilised ühendid lagunevad erineva kiirusega. Elusloodusele võõrad orgaanilised ühendid, orgaanilise keemia saadused nagu plastid, polüetüleenkile jne ei lagune looduslikus aineringes nagu orgaanilised ained. Nende lagunemine toimub oluliselt pikema aja jooksul. Sellepärast saastavad, reostavad nad loodust. Ka teokarbid ja selgroogsete luud lagunevad aeglaselt. Luustike järgi saab uurida kauges minevikus toimunut. Nii näiteks uurivad paleoantropoloogid säilinud luustiku põhjal inimese evolutsiooni.
Biolagunemise kiirus oleneb keskkonnast, kus lagunev aine asub. Oluline on just vee ja hapniku sisaldus selles, samuti temperatuur. Vaakumis ja madalal (või vastupidi väga kõrgel) temperatuuril, kus mikrooragnismide elutegevus peatub, bioloogiline lagunemine ka lõppeb. Bioloogiline lagunemine vajab eluks võimalikku keskkonda (biosfääri keskkonda). Elu võibki defineerida kui sobivat, piisavalt stabiilset keskkonda universumis, kus on võimalik elusorganismide bioloogiline lagunemine. Bioloogilisele lagunemisele vastandub abiootiline lagunemine, lagunemine ilma elusorganismide abita. (Abiootilist lagunemist põhjustab ultraviolettkiirgus, gammakiirgus, radioaktiivsus jne.) Kui mingi aine võib laguneda mikroorganismide kaudu, nimetatakse seda biolagunevuseks (võimeks bioloogiliselt laguneda, inglise biodegradability).
Lagundamise aeg
| Produkt | Aeg |
|---|---|
| Õuna südamik | 1–2 kuud |
| Tavaline paber | 1–3 kuud |
| Paberrätik | 2–4 nädalat |
| Pappkarp | 2 kuud |
| Puuvillriie | 5 kuud |
| Plastkattega piimapakk | 5 aastat |
| Vahaga kaetud piimapakk | 3 kuud |
| Plekkpurk | 50–100 aastat |
| Alumiiniumist purk | 150–200 aastat |
| Klaaspudel | määratlemata(igaveseks) |
| Kilekott | 10–20 aastat |
| Pehme plast (pudel) | 100 aastat |
| Kõva plast (pudeli kork) | 400 aastat |
-
Muusika astmed ei ole noodid. Astmete redel algab 1. astmest ja lõppeb 8. astmega. Kõikide helistike heliredel algab 1. astmest. Astmetel...
-
EESTI RAHVAKALENDRI PÜHAD: JAANUAR Talvine kalapüük Mootse talus . ERA, Foto 17846. Kolmekuningapäev (6. I) Nuudipäev (7. I)...