Otsing sellest blogist
UUS!!!
Juveniilne artriit
Blogi, mis räägib kõigest, mis on Leonhardile oluline ja/või huvitav. Kommenteerige, tellige, lugege, nautige ja õppige. Juveniilne artriit ...
teisipäev, 1. juuli 2025
Tsiilid ehk ripsmed
esmaspäev, 30. juuni 2025
Glükoos
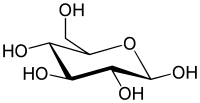
| Glükoos | |
|---|---|
   | |
| Lisateave Artiklis ei ole piisavalt viiteid. |
Glükoos ehk viinamarjasuhkur on monosahhariid, mis kuulub disahhariidide sahharoosi ja laktoosi koostisse. Glükoos tekib taimedes fotosünteesi tulemusena.
Glükoos on püsisoojaste loomade eelistatud energiaallikas. Nad varuvad glükoosi lihastesse ja maksa glükogeeni kujul.
Glükoos on tselluloosi polümeerse molekuli elementaarlülina oluline taime rakukesta komponent. Taimede glükoosivarud on tärklise kujul põhiliselt seemnetes ja mugulates.
reede, 27. juuni 2025
Protoplast
Protoplast on rakuseinaga raku "elus osa". See hõlmab rakutuuma ja protoplasmat.
Sellesse ei kuulu muu hulgas rakukest, varuained ja eritusained.
Taimeraku protoplast silsaldab membraan-, fibrillaar- ja makromolekulaarseid struktuure (kromosoomid, ribosoomid). Need paiknevad tsütosooliks nimetatavas vedelikus.
neljapäev, 26. juuni 2025
Amitoos
Amitoos (ka lihtpooldumine) on otsene raku- või rakutuuma jagunemine ilma mitoosile omaste protsessideta. Jagunemine toimub enamasti rakutuuma läbinöördumisega, kusjuures ei teki käävi.
Enne amitoosi toimub sageli rakutuuma suurenemine ja kromosoomide arvu kordistumine.
Looduses esineb amitoosi ainuraksetel ja teistel alamatel organismidel.
kolmapäev, 25. juuni 2025
Tuumamembraan
reede, 20. juuni 2025
Calvini tsükkel
Calvini tsükkel ehk Calvini-Bensoni tsükkel ehk Calvini-Bensoni-Basshami tsükkel on kõrgemate taimede kloroplastides tsükliliselt toimuvate fotosünteesi pimedusstaadiumi ensümaatiliste reaktsioonide jada, mis toimub kloroplasti stroomas. Protsessi käigus seotakse õhulõhede kaudu taimesse sisenenud CO2 ning moodustatakse sahhariide, kasutades valgusstaadiumi reaktsioonide tulemusena tekkinud kõrge energiaga NADPH ja ATP molekule. Ühe Calvini tsükli ringiga fikseeritakse üks CO2 molekul, milleks kulub 3 ATP ja 2 NADPH molekuli, mistõttu ühe glükoosi molekuli loomiseks peab Calvini tsükkel tegema kuus ringi.
Pimedusstaadiumiks nimetatakse osa fotosünteesi protsessist, mille juures ei ole valguse olemasolu vajalik. Calvini tsükli kõrvalproduktina moodustunud hapnik loob obligatoorse keskkonna Maa elusorganismidele, samuti on pimedusstaadiumi jooksul tekkinud monosahhariid glükoos aluseks terve biosfääri toiduahelale, olles püsisoojaste loomade eelistatud energiaallikas.
Protsessis eristatakse kolme olulist etappi: karboksüülimine ehk süsiniku sidumine, redutseerimine ning regenereerimine ehk süsiniku taastekitamine. Selle jooksul toimub CO2 fikseerimine RuBisCo reaktsioonis, 3-fosfoglütseraadi redutseerumine suhkruteks ning ribuloos-1,5-bisfosfaadi regenereerimine. Reaktsioonideks vajalikku vesinikku saadakse Calvini tsükli jaoks veest ja väävelvesiniku fotolüüsist.
Ajalugu
Calvini tsükli olemuse tegid kindlaks Melvin Calvin, Andrew Benson ning James Bassham 1950. aastal. Melvin Calvin pälvis tehtud töö ning tsükli mõtestamise eest 1961. aastal Nobeli auhinna. Tema eksperiment nägi ette radioaktiivse süsiniku 14C kasutamist märgisena, eesmärgiga kaardistada süsiniku teekond läbi taime terve fotosünteesi jooksul. Vaadeldi radioaktiivse süsiniku teekonda alates atmosfäärse süsinikdioksiidi absorptsioonist selle muundumiseni süsivesikuteks. Calvini ja tema meeskonna eksperimendis kasutati märgise jälgimiseks Chlorella kultuuri. Esimesi süsinikdioksiidi fikseerimise produkte analüüsiti paberkromatograafia ja autoradiograafia abil.
Protsess
Karboksüülimine
Karboksüülimise ehk süsiniku sidumise etapi eesmärgiks on süsiniku ja hapniku aatomite sidumine süsivesiku eelühenditesse. Seda protsessi katalüüsib oluline ensüüm ribuloos bisfosfaadi karboksülaas/oksügenaas ehk RuBisCo. Tegemist on levinuima ensüümiga maakeral. Taimedes on RuBisCo multimeerne valk, mille koosseis on L8S8, täpsemalt 8 suurt subühikut (L, 477 aminohappejääki) ning 8 väikest subühikut (S, 123 aminohappejääki). Sealjuures ei ole väikese subühiku spetsiifiline otstarve veel siiani selge, kuid on võimalik, et nende subühikute omavahelised interaktsioonid reguleerivad katalüüsi.
Süsiniku sidumisel toimub süsihappegaasi fikseerimine 5-süsinikulise sahhariidi ribuloos-bisfosfaadi RuBP vahendusel. See seob enda külge ensüümi RuBisCo. Toimub reaktsioon: RUBP + CO2 = 2 3-fosfoglütseraat (3PG). Seega ribuloos-1,5-bisfosfaadi ja CO2 sidumise tulemusena moodustub kuuest süsinikust koosnev labiilne vaheprodukt, mis laguneb vee toimel kaheks fosfoglütseraadi molekuliks.
Redutseerimine
Ribuloos bisfosfaadi karboksülaasi reaktsiooniprodukt 3PG konverteeritakse glütseeraldehüüd-3-fosfaadiks. Selleks katalüüsib fosfoglütseraadi kinaas anorgaanilise fosfaadi (Pi) ülekannet ATP koosseisust 3-fosfoglütseraadi karboksüülile, mille tulemusena tekib 1,3-bisfosfoglütseraat. Seejärel katalüüsib glütseeraldehüüd-3-fosfaat 1,3-bisfosfoglütseraadi karboksüüli redutseerimist aldehüüdks koos anorgaanilise fosfaadi eraldumisega. Protsessi tulemusena tekib glütseeraldehüüd-3-fosfaat.
Regenereerimine
Regenereermisel ehk süsiniku taastekitamisel jääb üks redutseerimise etapis saadud glütseeraldehüüd-3-fosfaadimolekul aldehüüdsesse vormi ning teisel liigutatakse karbonüülrühm otsmise süsiniku aatomi juurest keskmise süsiniku juurde. Seega muutub aldehüüd ketoühendiks, mille tulemusel tekib dihüdroatsetoon-fosfaat. Seejärel ühendab ensüüm aldolaas muudetud (ketoühenditest) ja muutmata (aldehüüdidest) 3-süsinikulised molekulid kokku 6-süsinikuliseks fruktoos-1,6-bisfosfaadiks. Sellest moodustub fruktoos-6-fosfaat, kus üks osa kulub RuBP regenereerimiseks ning teine osa muutub glükoosiks. Fruktoos-6-fosfaat muudetakse ATP energia abil vaheühendi ribuloos-5-fosfaadi kaudu ribuloos-1,5-bisfosfaadiks.
Calvini tsüklit limiteerivad tegurid
Calvini tsüklisse siseneva ning sealt väljuva süsiniku voog on dünaamilises tasakaalus, kuid üldine voolusuhe sõltub limitatsiooni ulatusest. Tulenevalt tsükli keerulisest ehitusest ei mõju erinevad tegurid lineaarselt, see tähendab, et muutus ühes osas ei põhjusta proportsionaalset suurenemist teises osas. Näiteks vähendades proteiini sisaldust ei mõju see lineaarse muutusena aktiivsuses, kuid võib toimuda lüke kas substraadi või produktide kontsentratsioonis, samuti ensüümi aktivatsiooni osas. Aktivatsioonitaset saab muuta langetades proteiini osakaalu kloroplastides ja lehtedes, ning samaaegselt takistades valku kodeeriva geeni normaalset ekspressiooni teda blokeerivate ensüümidega.
RuBisCo
RuBisCo ehk ribuloos-1,5-bisfosfaadi karboksülaasi/oksügenaasi peetakse maailma levinuimaks valguks ja suurima biomassiga ensüümiks. See ensüüm on suhteliselt aeglase katalüüsikiirusega, mille üheks peamiseks funktsiooniks on kõigi organismide elutegevuseks vajaliku süsiniku fikseerimine süsinikdioksiidina. Siiski ei ole RuBisCo märkimisväärselt substraadispetsiifiline, mistõttu toimub süsinikdioksiidi fikseerimisele lisaks ka hapniku seondumine. RuBisCo osakaal taime lehe koguvalgu juures on ligi pool. Katalüüsides üht olulisimat biokeemilist reaktsiooni, osa Calvini tsüklist, on tegemist äärmiselt universaalse kompleksiga. Toimub Calvini tsükli esimene reaktsioon, pöördumatu ribuloos-1,5-bisfosfaadi karboksüleerimine, selle tulemusena tekib kaks 3-fosfoglütseraadi molekuli, mida hiljem kasutatakse taimes suhkrute sünteesiks. 3-fosfoglütseraat on üks tähtsaim komponent suhkrute sünteesiks, seetõttu on RuBisCo ensüümil eluslooduse protsessides võtmeroll.
RuBisCo aktiivsus
Süsinikdioksiidi sidumise hulka määravad nii RuBisCo hulk kui ka ensüümi aktiivsustase. Alles loodud RuBisCo peab aktiivsuse saavutamiseks kõigepealt kasutama aktivaatormolekulidena CO2 ja Mg2+ ioone, samuti valgulise komponendina RuBisCo aktivaasi (RbcA). Edasi seondub RuBisCo suure subühiku Lys 201 jäägile CO2, millele omakorda seotakse Mg2+. Ensüümi aktiivsuse määramine on komplitseeritud, sest ühe molekuli kõik kaheksa katalüütilist tsentrit ei pruugi olla aktiveeritud samal ajal, lisaks ei ole nende funktsioneerimine sünkroonne. Lisaks sõltub RuBisCo koguaktiivsus ka valguse intensiivsusest, sest sellega kaasneb elektronide transport membraanil ning pH muutumine kloroplastis. Ensüümi aktiivsus on suurem valges, sest RuBisCo aktiveerumisel osalev RuBisCo aktivaas vajab funktsioneerimiseks ATP-d. Näiteks on enamikul taimedel RuBisCo spetsiifiline aktiivsus pimedas 25–50% sellest, mis kõrge valguse intensiivsuse juures. Substraadi kontsentratsioon mängib olulist rolli, näiteks kaasneb CO2 elimineerimisega lehele juhitavast gaasisegust RuBisCo vähenemine neljandiku võrra, kuid esialgne aktiivsus taastus pärast CO2 keskkonda lisamist umbes 30 minuti jooksul. Lisaks omavad kaasmõju ensüümi aktiivsusele ka strooma fosfaatioonide kontsentratsioon. Fosfaadi defitsiidiga kasvukeskkonnas kaasneb lisaks CO2 sidumise määra langus aga ka karboksüleerimise efektiivsuse vähenemine. See mõjutab RuBisCo aktiivsust just RuBP regenereerimise jõudluse läbi.
Transporterid
Kloroplasti kesta välimisel membraanil on transportervalgud, mis lasevad substraate massiga kuni 10 kDA vabalt difuseeruda sisemembraani. Kõik Calvini tsükli produktid peavad selle läbima. Protsessi aitavad spetsiifilised translokaatorid, mis on protsessis aktiivses vahetuses ning reguleerivad mitmeid aspekte raku metabolismis. Üks enim uuritud translokatsiooni süsteeme on fosfaat-trioonis ja fosfaat-fosfoglütseraat translokaator. Seda nimetatakse trioosfosfaadi anorgaanilise fosfaadi translokaatoriks.
neljapäev, 19. juuni 2025
Oksüdatiivne stress
Oksüdatiivne stress on olukord organismis, kus on häiritud oksüdatiivsete stressorite ja antioksüdantide omavaheline tasakaal. Ülekaalus on oksüdatiivsed stressorid, mis on kahjustavad tegurid. Teatud lühiajaline mõõdukas hästi kontrollitud oksüdatiivne stress on normaalne ja vajalik organismi kaitsemehhanismide käivitamiseks. Kestev sügav oksüdatiivne stress võib põhjustada või süvendada mitmesuguseid haigusi, nagu vähk, kardiovaskulaarsed haigused, ateroskleroos, hüpertensioon, isheemia-reperfusioonikahjustused, suhkurtõbi, närvisüsteemi kahjustavad haigused (Alzheimeri tõbi ja Parkinsoni tõbi) ning reumatoidartriit.
Oksüdatiivse stressi efektid
Väga tugevad ärritused põhjustavad nii ainevahetuslikke kui morfoloogilisi kohastumusreaktsioone rakus, misjärel tekib uus püsiv seisund, kus raku elutegevus on säilinud, kuid tema funktsioon on muutunud. Rakk kahjustub siis, kui tema kohandumisvõimalused etioloogilise teguri toime suhtes pole piisavad. “Rakukahjustusest saavad alguse kõik organikahjustuse vormid.” (Rudolf Virchow).
Oksüdatiivne stress on seotud oksüdeerivate ühendite hulga suurenemisega või antioksüdantsete kaitsemolekulide, nagu glutatioon, efektiivsuse olulise vähenemisega. Oksüdatiivse stressi efekt sõltub nende muutuste ulatusest. Väikestest muudatustest suudab rakk üle saada ja taastada oma algse oleku. Vahel võib isegi mõõdukas oksüdatsioon vallandada apoptoosi, samas kui intensiivsem stress võib põhjustada nekroosi.
Üheks tähtsamaks rakukahjustuse põhjuseks on vabade radikaalide kuhjumine. Vaba radikaal on keemiline ühend, mille välisorbiidil on üks paardumata elektron. Vabad radikaalid tekivad rakus:
- kiirgusenergia neeldumisel (UV-kiirgus, röntgenikiirgus);
- kehasisestes metaboolsetes oksüdatsiooniprotsessides;
- kemikaalide ja ravimite ainevahetuses.
Vabad radikaalid kahjustavad lipiide, mille tulemusel muutub rakumembraani, mitokondrite ja endoplasmaatilise retiikulumi membraanide struktuur, kaob membraanide võime reguleerida transmembraanseid ioongradiente. Kahjustuvad ka tsütoskleleti valkude struktuur, häiruvad geneetiline aparaat ja ensüümide struktuur.
•OH radikaal on kõige reaktiivsem vaba radikaal, mida bioloogilistes süsteemides leida võib. Ta reageerib enamiku biomolekulidega difusioonlimiteeritud kiirusel ning on võimeline põhjustama tõsiseid kahjustusi tekkimiskohast väikese raadiuse piirides. Võrreldes •OH-ga on •O2- väiksemat kahju tekitav vaba radikaal, reageerides väheste biomolekulidega. Teisalt võib•O2- kiiresti reageerida NO•-ga, andes peroksünitriti (ONOO-), mis on potentsiaalselt väga kahjulik, kuna võib genereerida hüdroksüülradikaale. Vesinikperoksiid võib oksüdeerida otseselt intratsellulaarseid komponente, kuid võrreldes eelnevatega on see tunduvalt vähem reaktiivne ühend. Ta on võimeline difundeeruma rakus ja rakkude vahel ning membraane läbima. H2O2 olulisus seisneb selles, et reageerides siirdemetallidega moodustub •OH. •OH ründab nii nukleiinhappeid, lipiide kui valke, samas kui •O2- ja H2O2 ei ründa DNAd ega algata lipiidide peroksüdatsiooni. Valgud kahjustuvad reaktiivsete hapnikuühendite toimel kas nende tioolrühmade oksüdatsioonil või teiste valgu koostises olevate aminohapete keemilisel modifikatsioonil.
Põhilised reaktiivsed ühendid
| Oksüdant | Iseloomustus |
|---|---|
| •O2-, superoksiidanioon | Ühe paardumata elektroniga hapnikuradikaal. Tekib mitokondrite hingamisahelas molekulaarse hapniku üheelektronisel taandamisel ja ka NADPH oksüdaasi reaktsioonil fagotsüütide välismembraanil.[4] |
| H2O2, vesinikperoksiid | Tekib superoksiidaniooni ja vesiniku reaktsioonil ensüümi superoksiiddismutaas (SOD) katalüüsil. Ei ole ise radikaal, kuid on prekursoriks aktiivsete radikaalide tekkel. On lipiidides lahustuv, seega difundeerub läbi raku struktuuride, põhjustades radikaalide tekkimist ka mujal kui mitokondris.[8] |
| •OH, hüdroksüülradikaal | Moodustub Fentoni reaktsioonil ja peroksünitriti lagunemisel. Äärmiselt reaktiivne.[7] |
| HOCl, hüpokloorishape | Moodustub vesinikperoksiidi ja kloori reaktsioonil müeloperoksidaasi katalüüsil neutrofiilides. Oksüdeerib valkude tioolrühmi, trüptofaani ja metioniini. |
| ONOO-, peroksünitrit | Moodustub kiirel mitteensümaatilisel reaktsioonil •O2- ja NO vahel. Reageerib metalloensüümide keskmes asuvate siiredemetallidega (näiteks Fe-S klastris). Algatab lipiidide peroksüdatisooni. Nitreerib trürosiini, oksüdeerib valkude tioolrühmi, trüptofaani, metioniini ja histidiini. Läbib membraane. |
Reaktiivsete hapnikuühendite (ROS) allikad
Üks reaktiivsete hapnikuühendite allikas normaalsetel tingimustel on nende lekkimine mitokondrist oksüdatiivsel fosforüleermisel. On hinnatud, et 3–5% kogu elektronide voolust viib reaktiivsete hapnikuühendite moodustamisele. •O2- tootmine võib toimuda ka spetsiifiliste ensüümide toimel (eelkõige oksüdaaside) ning puriinide (ksantiini oksüdaas), katehhoolamiinide (monoamiini oksüdaas), prostanoidide (lipoksügenaas) ja ksenobiootikumide (tsütokroom P450) metabolismil.
Reaktiivsed hapnikuühendid võivad eelmainitud reaktsioonides tekkida Ca2+ homöostaasi häirete, trauma või isheemia tagajärjel. Peamine •OH moodustumise allikas on H2O2 reaktsioon siirdemetalliioonidega, nagu Fe2+ või Cu2+ (Fentoni reaktsioon) või Fe2+ katalüüsitud reaktsioon H2O2 ja •O2- vahel (Haberi-Weissi reaktsioon). Hüdroksüülradikaalid tekivad ka preoksünitritist, mis füsioloogilisel pH-l laguneb. H2O2 moodustub •O2- dismutatsioonil, mida katalüüsib ensüüm superoksiidi dismutaas. H2O2 moodustub ka teiste oksüdaasensüümide toimel (näiteks aminohapete oksüdaasid).
Lämmastikoksiid (NO•) sünteesitakse aminohappest L-arginiin ensüümi lämmastikoksiidi süntaas katalüüsil endoteeli rakkudes (kui vaskulaarse toonuse regulaatorit), samuti ka paljudes teistes rakutüüpides (kui sekundaarset signaalmolekuli).
Aktiveeritud fagotsüüdid on võimelised genereerima •O2-, H2O2, HOCl ja NO• ühendeid, mis kõik võivad kaasa aidata koekahjustuse tekkele põletikuprotsessis.
Oksüdatiivne stress ja haigused
Oksüdatiivset stressi peetakse oluliseks neurodegeneratiivsete haiguste patogeneesis, nagu Lou Gehrigi haigus (ehk motoneuroni haigus), Parkinsoni tõbi ja Alzheimeri tõbi Oksüdatiivset stressi seostatakse ka kardiovaskulaarsete haigustega, kuna madala tihedusega lipoproteiinide (LDL) oksüdatsioon endoteelis on prekursoriks kolesterooli ladestusele. Oksüdatiivne stress mängib ka rolli biokeemilises kaskaadis hüpoksiajärgse reperfusioonikahjustuse tekkel. Oksüdatiivne stress süvendab koekahjustust hüperoksiajärgselt ka diabeedi korral.
Oksüdatiivne stress on tõenäoliselt seotud kõrgest vanusest tulenevate vähkkasvajate moodustumisega. Aktiivsed ühendid võivad otseselt kahjustada DNA-d ja seega olla mutageensed ning samuti võivad maha suruda apoptoosi, indutseerida proliferatsiooni, invaseerumist ja metastaasi. Helicobacter pylori põhjustatud põletik, mille tõttu suureneb reaktiivsete hapniku- ja lämmastikuühendite tootmine maos, on oluline tegur maovähi tekkes.
Antioksüdandid lisanditena
Antioksüdantide manustamine haiguste ennetamiseks on leidnud vastakaid arvamusi. Suure riskiga gruppides, nagu seda on suitsetajad, võib suur doos sünteetilist beetakaroteeni kopsuvähki haigestumise tõenäosust suurendada. Väiksema riskiga grupis tundub E-vitamiini kasutamine vähendavat südamehaiguste väljakujunemise riski. Toit sisaldab laia valikut karotinoide ja E-vitamiine (tokoferoole ja tokotrienoole), seega ex post facto epidemioloogiliste uuringute tulemused võivad erineda pärast tehislikke eksperimente tehtud järeldustest, kuna viimasel juhul kasutatakse isoleeritud aineid. Siiski on ravimifirma AstraZeneca väljatöötatud radikaale eemaldav nitroonipõhine ravim NXY-059 näidanud efektiivset toimet insuldi tagajärgede ravis.
Immuunkaitse
Immuunsüsteem kasutab ära oksüdantide letaalseid efekte, tootes oksüdeerivaid ühendeid patogeenide tapmiseks. Aktiveerunud fagotsüüdid toodavad hapniku ning lämmastiku reaktiivseid ühendeid, nende seas •O2- ja •NO ja ONOO- Kuigi nende väga reaktiivsete ühendite kasutamine fagotsüütide tsütotoksilises vastuses kahjustab ka oma kudesid, on oksüdantide mittespetsiifilisus eelis, kuna kahjustab märklaudraku peaaegu igast aspektist, vältides olukorra teket, kus patogeen pääseb sellise immuunvastuse käest ühe märklaudmolekuli mutatsiooni abil.
Kaitsemehhanismid vabaradikaalse kahjustuse vastu
Mitokondrite roll hapniku vabade radikaalide tekke kontrollis
- Hapnikuradikaalide teke ja nendest vabanemine
Mitokondrid tõkestavad hapniku vabade radikaalide kahjustust sel viisil, et redutseerivad enamiku molekulaarsest hapnikust veeks, kandes üle neli elektroni. 1–3% juhtudest taandatakse tarvitatud hapnik üheelektronilise ülekandega, tekib superoksiid. See protsess leiab aset hingamisahela alguses ja keskosas, kus asuvad reaktiivsed elektroni ülekandjad (flaviinid, CoQ), mis elektroni sidudes muutuvad ise vabaradikaaliks (nt CoQ•- vabaradikaal). Superoksiid tehakse kahjutuks mitokondri ensüümi MnSOD abil. Moodustub H2O2, mis difundeerub kergesti läbi mitokondrite ja rakumemebraani ning lahustub kudedes. H2O2 lokaalne kontsentratsioon langeb kiiresti koos superoksiidi kahjustav toimega.
- Oksüdatsiooni ja fosforüleerimise kerge lahutamine
Mida suurem on mitokondrite membraanipotentsiaal, seda suurem on CoQ•- radikaali tekkekiirus ning hapniku vabade radikaalide teke. Kui ATP sünteesi kiirus mitokondrites on madal, näiteks lihasraku puhkeoleku seisundis, mil membraanipotentsiaal on maksimaalne, on superoksiidide tekkevõimalus suurem. Intensiivse ATP sünteesi juures (raske füüsilise töö puhul), mil membraanipotentsiaal on vähenenud, on superoksiidi moodustumise tõenäosus väiksem. Normaalselt talitlevas puhkeolekus rakus pidurdavad hapniku vabade radikaalide teket türeoidhormoonid ja vabad rasvhapped, mis soodustavad prootonite tagasileket mitokondri maatriksisse ning aitavad hoida membraanipotentsiaali hapniku vabade radikaalide tekkimiseks vajalikust lävest madalamal tasemel. Seega toimub oksüdatsiooni ja fosforüülimise lahutamine, millel on mitokondriaalse antioksüdantse kaitse mehhanismis oluline roll. Membraanipotentsiaali vähenemisel ei saa organism enam sünteesida ATPd. See on hind, mis tuleb organismil maksta sellist laadi kaitse eest.
- Tsütokroom c roll
Kui vaatamata oksüdatsiooni ja fosforüleerimise kergele lahutamisele •O2- siiski tekib, oksüdeerub mitokondrite intramembraanses ruumis paiknev tsütokroom c: CytC3+ + •O2- → CytC2+ + O2. Redutseeritud tsütokroom c (CytC2+) oksüdeerib uuesti hapnik tsütokroomoksüdaasses reaktsioonis. Võrrandist on näha, et tsütokroom c eemaldab superoksiidi ja taastoodab molekulaarse hapniku. See mehhanism on eriti tõhus siis, kui tsütokroom c väljub mitokondri välismembraani kahjustusel mitokondritest tsütoplasmasse. Seega tsütokroom c mitte ainult ei indutseeri apoptoosi, vaid avaldab ka antioksüdatset toimet.
Teised oksüdatiivset stressi limiteerivad mehhanismid
- Vabu radikaale konverteerivatest ensüümidest
on tähtsad mitokondriaalsed MnSOD ja tsütoplasmaatiliselt paiknevad superoksiidi dismutaas CuZnSOD ja katalaas ning glutatiooni peroksüdaas (katalüüsib vesinikperoksiidi taandamist glutatiooni oksüdatsiooni arvel). Nende ensüümide ekspressioon südamelihases hüpoksia/reoksügenisatsiooni-kahjustusel muutub oluliselt: kroonilise hüpoksia faasis nende ensüümide hulk väheneb, kuid reoksügenisatsioonifaasis (reperfusiooni) kasvab ja see muutus soodustab müokardi kaitset hapniku vabade radikaalide kahjustuse eest isheemiajärgsel reperfusioonil.
- hapniku vabade radikaalide kuhjumist aitavad peatada paljud niinimetatud radikaalide sidujad.
- Raku vesifaasis on olulised taandatud glutatioon ja askorbaat; membraanifaasis tokoferool, karotenoidid ja ubikinool (CoQH2).
Eoseline paljunemine
Eoseline sigimine ehk sporogoonia on suguta sigimisviis, mis toimub eriliste paljunemisrakkude ehk eoste abil.
Eoseline sigimine esineb mõningatel protistidel (eosloomad) ning kõikidel taimedel ja seentel.
kolmapäev, 18. juuni 2025
Aktinobakterid
| Aktinobakterid | |
|---|---|
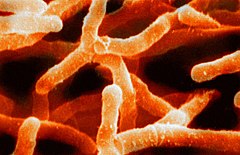 Actinomyces israelii | |
| Taksonoomia | |
| Riik | Bakterid Bacteria |
| Hõimkond | Actinobacteria |
Kaks grampositiivsete bakterite hõimkonda – Actinobacteria ja Firmicutes – on valgujärjestusel põhinevate analüüside järgi ühed vanimad bakterite hõimkonnad. Aktinobakterite eristumine teistest hõimkondadest on evolutsiooniliselt nii ürgne sündmus, et neile fülogeneetiliselt lähimat rühma ei ole võimalik kindlalt tuvastada.
Aktinobakterid on tänapäevase süstemaatika järgi üks suurmaid hõimkondi, mis eristub teistest hõimkondadest 16S rRNA analüüsi põhjal. Selle alusel on hõimkond jagatud 6 klassiks, 18 seltsiks, 39 sugukonnaks ja 130 perekonnaks.
Varem nimetati aktinobaktereid ekslikult seenteks nende sarnase eluviisi tõttu. Pinnases elutsevad aktinobakterid moodustavad mütseelisarnaseid agregaate ja lagundavad surnud organisme taimedele kättesaadavaks orgaaniliseks aineks. Seetõttu nimetati neid varem näiteks kiirikseenteks.
Aktinobakterid on laialt levinud nii maismaa kui ka vesikeskkonna ökosüsteemides. Tänu hõimkonna mitmekesisusele kasutatakse selle esindajaid väga paljudes eri valdkondades.
Omadused ja morfoloogia
Aktinobakterite hõimkond koosneb hargnevatest üherakulistest mikroorganismidest, kellest enamik on aeroobsed ja moodustavad kas substraadi- või õhumütseeli. Nad moodustavad spoore, sporangiume ja sporangiospoore. Spoorid on morfoloogiliselt ümarad kuni piklikud, liikuvad spoorid on varustatud ühe või mitme viburiga. Aktinobakterite morfoloogiline ehitus on kompaktne, koloonia pind on kuiv ja tihti kaetud õhumütseeliga. Aktinobakterite identifitseerimiseks on lisaks mütseeli ja spooride moodustamisele kasutatud ka pigmendi tootmist. Actinobacteria hõimkonna esindajate kasv on enamasti aeglane ja nende eraldamiseks mullast ning kultiveerimiseks laboris tuleb seega pärssida kiiresti kasvavate bakterite ja seente areng.
Mitmekesisus
Genoomiuuringud
Peamised geneetilised mehhanismid, mis aktinobakterite genoomi suurust ja kuju mõjutavad on geeni duplikatsioon, horisontaalne geeniülekanne, geenide kadu ja kromosomaalsed ümberkorraldused. Viimased uuringud näitavad, et geeniduplikatsioonidel on evolutsioonis arvatust väiksem efekt. Horisontaalse geeniülekande tõestusi on aktinobakteritel mitmeid. Näiteks Corynebacterium diphtheriae faagid kannavad oma genoomis suurt difteeria toksiini geeni, Mycobacterium ulcerans’i lineaarne plasmiid kannab makroliidi toksiini geene, mis vastutavad haavandite tekkimise eest ja Mycobacterium tuberculosis tüvi Rv0986-8 virulentsusoperon on tulnud horisontaalselt tuberkuloositekitaja eellaselt (Mycobacterium prototuberculosis). Genoomi degradatsioon on tõestatud näiteks leepratekitajal – võrreldes tuberkuloositekitajaga on tal umbes 1000 geeni vähem. Lisaks on leepratekitajal leitud palju pseudogeene, mis viitab sellele, et geenide kadumine jätkub ka praegu. Kromosomaalsed ümberkorraldused toimuvad korduvate mobiilsete järjestuste abil (näiteks transposoonid, plasmiidid jne). Bakterigenoomid, milles esineb rohkem korduvjärjestusi, on suuremate ümberkorraldustega. Taksonitevaheliste erinevusteni viib nende järjestuste vaheline homoloogiline rekombinatsioon.
Aktinobakteritel on unikaalne molekulaarne sünapomorf – homoloogiline, umbes 100 nukleotiidi pikkune insertsioon 23S rRNA geeni 54. ja 55. heeliksi vahel.
Genoomi sekveneerimine
Esimene sekveneeritud aktinobakteriaalne genoom oli inimese tuberkuloositekitaja (M. tuberculosis) tüvi H37Rv. Pärast seda on sekveneeritud veel umbes 20 Actinobacteria hõimkonna esindaja genoomi, mõne puhul isegi mitu eri tüves. Sekveneerimine näitas streptomütseetide eripära – neil on tavalise tsirkulaarse genoomi asemel lineaarne genoom. Geelelektroforeesi abil on avastatud lineaarne genoom ka mõnelt veel sekveneerimata Actinobacteria rühmalt. Nende suurused jäid vahemikku 7,7–9,7 Mb. Aktinobakterite iseloomulike tunnustena leiti sekveneerimisel veel suurte lineaarsete plasmiidide esinemine genoomis. Neil plasmiididel on tüüpilised lühikesed pööratud kordused 5'-otsades.
Vegetatiivne paljunemine
Vegetatiivne sigimine on suguta sigimisviis, kus uus organism saab alguse ühest vanemorganismist, sageli tema (keha)osa(de)st. Vegetatiivne sigimine on suguta sigimise üks kahest peamisest tüübist (teine on eoseline sigimine).
Vegetatiivne sigimine esineb nii ainuraksetel kui ka hulkraksetel organismidel. Ainuraksetel (arhedel, bakteritel jt) avaldub see rakujagunemisega (sealhulgas pooldumise, pungumise ja hulgijagunemisega). Hulkraksetele organismidel (sh taimedel, loomadel) avaldub vegetatiive sigimine ühe vanemorganismi mittegeneratiivse(te) ehk somatogeense(te) (keha)osa(de) eraldumisel, millest areneb uus organism (järglane). Ka hulkraksetele organismidel esineb pungumist (näiteks pärmseened, käsnad), pooldumist (ripsussid). Taimede puhul võib mittegeneratiivseks kehaosaks olla mugul, eriline sigikehake jt. Vegetatiivse sigimise erijuhtudeks on loomariigis rõngussidel esinev para- ja arhitoomia.
-
Muusika astmed ei ole noodid. Astmete redel algab 1. astmest ja lõppeb 8. astmega. Kõikide helistike heliredel algab 1. astmest. Astmetel...
-
EESTI RAHVAKALENDRI PÜHAD: JAANUAR Talvine kalapüük Mootse talus . ERA, Foto 17846. Kolmekuningapäev (6. I) Nuudipäev (7. I)...