Geenivektor ehk geenisiirdaja on geeniteraapias kasutatav rekombinantse DNA või RNA konstrukt, milles siiratav pärilikkusaine on ühendatud elementidega, mis võimaldab sellel rakku siseneda, seal integreeruda ja avalduda.
Geeniteraapias kasutatakse viiruslikke ja mitteviiruslikke vektoreid. Vektori valik sõltub sihtmärkrakust ja terapeutilise geeni omadustest, näiteks selle suurusest ja avaldumise ajast.
ViirusvektoridViiruslikud vektorid põhinevad viirustele omasel käitumisel tungida organismi rakku, seal paljuneda ning sisestada oma pärilikkusaine peremeesorganismi genoomi.
Viirusvektori konstrueerimisel asendatakse enamik viiruse pärilikkusainet terapeutilise geeniga, kuid seejuures säilitatakse viiruse nukleiinhapete osa, mis on vajalik rakule kinnitumise ja rakku sisenemise tagamiseks.
Kuigi viirusvektorid on geeni viimisel rakku efektiivsemad kui mitteviiruslikud vektorid, võib nende kasutamisega kaasneda viiruslik infektsioon. Peamised geeniteraapias kasutatavad viirused on retroviirus, adenoviirus, adenoassotsieerunud viirus, alfaviirus, herpesviirus ja vaktsiinia viirus. 2012. aasta seisuga oli inimese geeniteraapia näidetest umbes 70% sellised, kus DNA viimiseks kudedesse on kasutatud viirusvektoreid.
Viirusvektorite konstrueerimine
Viirusvektori konstrueerimisel arvestatakse, et ideaalne viiruslik vektor hõlmab kõiki viiruse infektsioonitsüklile omaseid tunnuseid, kuid samas tuleb vältida haigust põhjustavate geenide avaldumist sihtmärkrakus. Selleks asendatakse enamik viiruse pärilikkusaine terapeutilise geeniga, kuid seejuures säilitatakse viiruse nukleiinhapete osa, mis on vajalikud rakule kinnitumiseks, rakku sisenemise tagamiseks, pärilikkusaine pakkimiseks kapsiidi ning DNA terapeutilise geeni lülitamiseks raku genoomi. Neid geene nimetatakse cis-elementideks. Kustutatud viiruse geenid, mis on seotud replikatsiooni, kapsiidi- ja membraanivalkudega, paiknevad eespool nimetatud geenidest eraldi konstruktis, näiteks plasmiidis. Neid nimetatakse trans-elementideks. Seejärel viiakse vektorgenoom ja trans-elemendid pakkimisrakku ning seal moodustuvad rekombinantsed viirused, mis on võimelised terapeutiliset geeni rakku viima ja seda genoomi lülitama.
Vahel konstrueeritakse geeniteraapia tarbeks ka pseudotüpeeritud viirusi, mis suurendavad või vähendavad sihtmärkrakkude ampluaad. Näiteks populaarseim viirus, mida vektorite tarbeks kasutatakse, on Retroviridae perekonda kuuluv Simia immuunpuudulikkuse viirus, mis on kaetud vesikulaarset stomatiiti põhjustava viiruse G-valkudega.
Retroviirus
Retroviirus kasutab nukleiinhappena RNA-d ning kasutades oma nakatamistsüklis pöörtranskriptaasi, kodeerib see DNA-d. Viiruse kodeeritud DNA seostub stabiilselt sihtmärkraku geneetilise struktuuriga viiruse kodeeritud ligaasi vahendusel. Retroviirus on võimeline nakatama ainult jagunevaid rakke, seega terapeutilise geeni omadused kantakse edasi rakuliini pidi. Kuna retroviirus siseneb peremeesraku geenidesse suvaliselt, suurendab see vähitekke riski. Maksimaalne kogus pärilikkusainet, mida viirusse laadida võib, on 8000 aluspaari.
Retroviirusel põhinevat vektorit ja ühtlasi ka geeniteraapiat rakendati inimese puhul esmakordselt 1990. aastal ADA-SCID ehk adenosiini deaminaasi puudusest põhjustatud ägedat immuunpuudulikkust põdeval patsiendil. Adenosiini deaminaasi defektsuse korral koguneb T-lümfotsüütidesse desoksüadenosiin, mis on T-rakkudele toksiline, seega organismil ei teki immuunvastust ning haiged surevad lapseeas. Inimese ADA-geen klooniti retroviirusel põhinevasse vektorisse ning viidi haige lapse valgeverelibledesse, mis olid organismist eelnevalt eraldatud. Pärast ADA-geeni avaldumise kontrollimist viidi leukotsüüdid organismi tagasi.
2000. aastal rakendati 15 poisslapsel geeniteraapiat X-liitelise SCID vastu. Nende vereloome tüvirakkudesse viidi IL2Rye-geen. Selline ravimikatsetus osutus edukaks, kuid kahe aasta pärast haigestusid ravitutest kaks leukeemiasse. Neil kahel lapsel toimus seoses retroviiruse integratsiooniga translokatsioon 7. ja 11. kromosoomi vahel. Retroviiruse vektor oli koos terapeutilise geeniga integreerunud LMO2-geeni, mis kontrollib rakkude jagunemist, stimuleerides samuti selle avaldumist. Sellise kaasefekti tõttu keelustati vahepeal USA-s ning mitmes Euroopa riigis retroviirusel põhinev geeniteraapia.
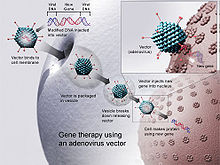
Viirusvektori seostumine rakumembraaniga ja pärilikkusaine toimetamine rakku
Adenoviirus
Adenoviirusvektorite eelis on see, et viiruse DNA, millest haigust tekitav osa on osaliselt kustutatud, suudab mahutada suhteliselt pikka DNA osa ehk umbes 7500 aluspaari. Samuti viivad nad rakkudesse palju viiruse osakesi ja mõjutavad nii puhkavaid kui jagunevaid rakke. Sellegipoolest toodavad nad mitmeid viirusele omaseid valke, mis võivad põhjustada immuunreaktsiooni, mis nii vektorid kui ka nende mõjutatud rakud kiiresti elimineerib. Adenoviirust kasutades ei õnnestu manustamise kordamine, kui esmakordsel vektori manustamisel kaasnes immuunsüsteemi muutus, mis surus maha esmase vastuse adenoviiruse kattevalkude vastu. Seega on adenoviiruste kasutamine geenivektorina ohtlik, kuna see võib patsiendi organismis põhjustada väga tugeva immuunvastuse. Näiteks patsient, kes kannatas ornitiini transkarboksülaasi defektsuse all ja kelle geeniteraapilisel ravil kasutati adenoviiruse vektorit, suri organismi ägeda immuunvastuse tõttu.
Adenoviiruste kaksikahelalist DNA-d ei lülitata sihtmärkraku genoomi, vaid see jääb rakutuumas eraldiseisvaks. Seega terapeutiline geen ei jagune rakkude paljunemisel.
Adenoviirusel arvatakse olevat suur potentsiaal vektorina vähivastases geeniteraapias. 2003. aastal tuli Hiinas turule ravim Gendicine, milles kasutatav p53 tuumorsupressorgeen ravib lamerakulist kartsinoomi.
Adenoassotsieerunud viirus
Adenoassotsieerunud viiruste vektorid kasutavad nukleiinhappena üheahelalist DNA-d, nakatades efektiivselt jagunevaid ja mittejagunevaid rakke. Viiruste vektorid integreeruvad genoomi arvatavasti juhuslikult, kuigi mõned originaalviirused integreeruvad peamiselt 19. kromosoomi teatud piirkonnaga. Seepärast on nende puhul samasugune oht onkogeeni aktiveerimiseks nagu retroviirusvektorite puhul. Adenoassotsieerunud viirusega on võimalik transportida pärilikkusainet suurusega kuni 4500 aluspaari. Seda vektorit on kasutatud peamiselt lihas- ja silmaprobleemide korral.
Alfaviirus
Alfaviirus kasutab nukleiinhappena RNA-d, nakatades jagunevaid ja mittejagunevaid rakke. Maksimaalne kogus pärislikkusainet, mida selle vektoriga transportida saab, on 7500 aluspaari. Alfaviiruste kasutamine geeniteraapias on piiratud, kuna nad suudavad seonduda väheste rakkude retseptoritega ja nende ekspressioon on lühike.
Herpes simplex'i viirus
Herpes simplex'i viirus kasutab nukleiinhappena üheahelalist DNA-d, nakatades nii jagunevaid kui ka mittejagunevaid rakke. Maksimaalne kogus pärilikkusainet, mida selle vektoriga transportida saab, on 30 000 aluspaari. Seda viirust on kasutatud vektorina glioomi, melanoomi ja munasarjavähiga patsientidel. Kuna herpesviirus on neurotroofiline, siis kasutatakse herpesviirusel põhinevaid vektoreid kõige enam terapeutilise geeni saatmiseks pea- ja seljaajju. Herpesviirus on väga transgeenne ning selle põhjal konstrueeritud vektorid võimaldavad pikka terapeutilise geeni püsimist organismis.
Vaktsiiniaviirus
Vaktsiiniaviirus kasutab nukleiinhappena kaheahelalist DNA-d. Maksimaalne kogus vaktsiiniaviirusega transporditavat pärislikkusainet on 25 000 aluspaari. Vaktsiiniaviirus ei integreeru sihtmärkraku genoomi, vaid replitseerub täielikult raku tsütoplasmas.
Mitteviiruslikud vektoridMitteviiruslike vektorite korral sisestatakse terapeutiline geen rakku füüsilisel või elektrokeemilisel teel. Võrreldes viiruslike vektoritega on mitteviiruslikud vektorid odavamad, neid on lihtsam toota ja need on vähem patogeensed. Lisaks võimaldavad mitteviiruslikud vektorid transportida suuremat kogust pärislikkusainet. Mitteviiruslike vektorite populaarsust pärsib nende väiksem efektiivsus võrreldes viirusvektoritega.
Füüsilised meetodid
Füüsiliste meetodite puhul rakumembraanid lõhutakse ja terapeutiline geen sisestatakse füüsiliselt sihtrakku. Peamised geeniteraapias kasutatavad füüsilised meetodid on geeni süstimine sihtrakku või veresoonde, ballistiline DNA, elektroporatsioon, sonoporatsioon, fotoporatsioon, magnetofektsioon ja
hüdroporatsioon.
Geenide süstimine
Terapeutilise geeni süstimine üksikusse keharakku või veresoonde on ohutuim meetod geeni ülekandmiseks. Teisest küljest pärsib selle meetodi populaarsust väike efektiivsus. Organismi immuunsüsteem elimineerib katmata eksogeense geeni kiiresti. Näiteks eksgeense plasmiidi poolestusaeg hiire organismis on 10 minutit, mis pole geenide avaldumiseks reeglina piisav. Seda meetodit on enim kasutatud naha-, südame- ja maksaprobleemide korral.
Ballistiline DNA
Ballistilise DNA meetod põhineb kulla- või hõbedaosakestega kaetud DNA tulistamisel geenipüssiga kõrge rõhu all sihtmärkrakku. See meetod võeti kasutusele 1980-ndate keskel ning kasutati esialgu markergeeni transportimiseks taimekudedesse. Seda meetodit kasutatakse munasarjavähi puhul.
Elektroporatsioon
Elektroporatsiooni korral tõstavad elektroporaatorid raku plasmamembraani elektrijuhtivust. Elektriline impulss tekitab plasmamembraanis ajutisi poore, mille kaudu saab terapeutiline geen rakku siseneda. Seda meetodit kasutatakse eelkõige naha- ja lihaskudede korral. Elektroporatsiooni negatiivseteks külgedeks on liiga suurte koekahjustuste tekitamine ning samuti ei pääse elektroodidega, millega rakumembraan lõhutakse, paljudele siseelunditele juurde.
Sono- ja fotoporatsioon
Sonoporatsioon on mitteinvasiivne kohtspetsiifiline meetod, mis kasutab ultrahelilaineid, mis augustavad rakumembraani, et geen saaks rakku pääseda. Fotoporatsiooni korral kasutatakse rakumembraani augustamiseks laserimpulssi.
Magnetofektsioon
Magnetofektsiooni korral seostatakse terapeutiline geen magnetiseeruvate nanoosakestega, mis sisestatakse tugeva magnetvälja toimel rakku. Magnetofektsioon on organismile ohutu, kuid vastava meetodi kasutamisel tuleb geeniteraapiat pidevalt korrata, kuna terapeutiline geen ei integreeru raku genoomi.
Hüdroporatsioon
Hüdroporatsiooni kutsutakse ka hüdrodünaamiliseks geeniülekandeks. See meetod kasutab hüdrodünaamilist rõhku läbimaks rakumembraani. Suure DNA kontsentratsiooniga lahuse süstimisel rakku luuakse hüdrodünaamiline surve, mille tulemusena tekib rakumembraanil juurde poore, mis hõlbustavad geeni levikut organismis ja seekaudu geeni jõudmist sihtmärkrakku.
Keemilised meetodid
Keemilised meetodid terapeutilise geeni sihtmärkrakku transportimiseks jagunevad anorgaanilisteks, lipiidseteks, valgulisteks ja polümeerseteks kandjateks. Selliste kandjate ülesanne on seostuda rakumembraaniga ning kaitsta terapeutilist geeni raku kaitsemehhanismide eest.
Anorgaanilised kandjad
Terapeutilised geenid kaetakse anorgaaniliste nanoosakestega, näiteks kaltsiumfosfaadi, kulla või räniga, mis tõhustavad terapeutilise geeni jõudmist sihtmärkrakku, madaldades organismi kaitsereaktsioonide mõju. Näiteks kullaosakestega kaetud geen, mis infrapunakiirguse mõjul rakumembraani läbib, on organismile vähem toksiline kui lipopleksid. Samas pole anorgaanilised kandjad biolagunevad, seega nad kuhjuvad rakkudesse ja pärsivad nende funktsiooni.
Oligonukleotiidid
Oligonukleotiidide ülesandeks geeniteraapias on pärssida pärilikku haigust põhjustava geeni avaldumist. Selle saavutamiseks eksisteerib mitmeid mehhanisme. Üheks võimaluseks on vigase geeni antisenss-spetsiifilisuse kasutamine, mis inhibeerib selle ekspressiooni. Võimalik on ka siRNA-de seostumine vigasele mRNA-le, mis pärsib valgusünteesi. Lisaks eelnenutele on väljatöötamisel kaheahelalised oligodeoksünukleotiidid. Ideaalis seonduksid transkriptsioonifaktorid vigase geeni promootori asemel vastavatele oligonukleotiididele, mis vähendaks sihtmärkgeeni avaldumist.
Lipoplekssed ühendid
Lipopleksne ühend koosneb lipiidist, millesse on pakitud geen. Lipiidil on positiivselt laetud hüdrofiilne pea ja hüdrofoobne saba. Lipiidi positiivselt laetud peaosa seostub elektrostaatilise interaktsiooni kaudu negatiivselt laetud geeniga, moodustades lipoplekse ühendi. Kuna lipopleks on positiivselt laetud, seostub see rakumembraanil olevate negatiivselt laetud glükoproteiinide ja proteoglükaanidega ning siseneb rakku. Lipiidikiht geeni ümber kaitseb geeni raku kaitsemehhanismide eest, kuid lipiidikihi laeng vähendab kaitse kestvust.
Rakku sisenevad peptiidid
Rakku sisenevad peptiidid on väikesed, sisaldades alla 40 aminohappejäägi. Need peptiidid on enamasti pärit viirusvalkudelt, mis tungivad rakku, seostudes mitmete rakumembraanivalkudega. Lisades lipiidsetele kandjatele kindlaid aminohappelisi järjestusi, võib kandja seonduda spetsiifiliselt mõne teatud organelliga.
Polümeersed kandjad
Kitosaan
Kitosaan on lineaarne katioonne polüsahhariid, mis on eraldatud krabidest ja krevettidest. Selle biolaguneva polümeeri toimeks on seostumine foolhappega ning on kahjutu ka suurte kontsentratsioonide juures.
Dendrimeerid
Dendrimeerid on korrapärase hargnenud struktuuriga positiivse pinnalaenguga polümeerid, mis läbivad endotsütoosi teel hõlpsalt rakumembraani. Dendrimeer seostub geeniga oma positiivse pinnalaengu tõttu füsioloogilise pH juures. Dendrimeeride laialdasemat kasutamist pärsib nende liigne spetsiifilisus seostumaks rakumembraanidega ja toksilisus.
Želatiin
Želatiin on looduslik biolagunev polümeer, mida kasutatakse laialdaselt farmaatsia- ja meditsiinivaldkonnas. See ühend koosneb denatureerunud kollageenist, millel on unikaalne aminohappeline sisaldus. Positiivse laenguga želatiin saadakse etüleendiamiini sisestamisel želatiini karboksüülrühma. Želatiini kasutamine geenivektorina on inimesele ohutu.
Hüaluroonhape
Hüaluroonhape on looduslik biolagunev polümeer, mis suudab sünteetilistest polümeeridest edukamalt terapeutilist geeni läbi rakumembraani transportida. Hüaluroonhapet kasutatakse sarv- ja võrkkestaprobleemide korral.
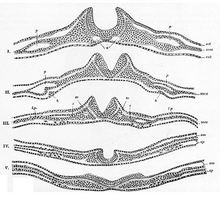
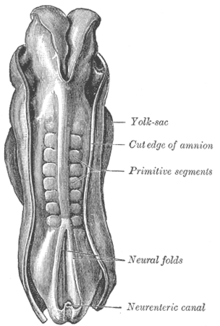
 See tekib pärast gastrulatsiooni ektodermiks (välimine iduleht) nimetatavast rakukihist embrüo pinnal, mis asetseb seljakeeliku kohal ja mille mõjul siin moodustub pisut paksem neuroektoderm kui neuraalplaat. See võlvub külgmiselt neuraalvallidega üles ja nende vahel piklikuks neuraalvaoks sisse. See järel voltub neuraalvagu neuraalvoltidega torujaks moodustiseks. Selle protsessi käigus, mida nimetatakse primaarseks neurulatsiooniks, moodustub sisse vajudes neuraaltoru, mis eraldub ektodermist, mis pinnaektodermina kesknärvisüsteemi voltunud alge kohal uuesti sulgub. Kummalgi pool neuraaltoru moodustuvad endise neuraalplaadi äärepiirkonna rakkudest ajutiselt neuraalharjad, millest hiljem saavad melanotsüütide (pigmendirakkude) kõrval perifeerse närvisüsteemi mitmesugused osad.
See tekib pärast gastrulatsiooni ektodermiks (välimine iduleht) nimetatavast rakukihist embrüo pinnal, mis asetseb seljakeeliku kohal ja mille mõjul siin moodustub pisut paksem neuroektoderm kui neuraalplaat. See võlvub külgmiselt neuraalvallidega üles ja nende vahel piklikuks neuraalvaoks sisse. See järel voltub neuraalvagu neuraalvoltidega torujaks moodustiseks. Selle protsessi käigus, mida nimetatakse primaarseks neurulatsiooniks, moodustub sisse vajudes neuraaltoru, mis eraldub ektodermist, mis pinnaektodermina kesknärvisüsteemi voltunud alge kohal uuesti sulgub. Kummalgi pool neuraaltoru moodustuvad endise neuraalplaadi äärepiirkonna rakkudest ajutiselt neuraalharjad, millest hiljem saavad melanotsüütide (pigmendirakkude) kõrval perifeerse närvisüsteemi mitmesugused osad.