Tsütokinees on raku jagunemisprotsessi etapp, mille käigus kromosoomid, tsütoplasma, organellid ja rakumembraan jagatakse võimalikult võrdselt kahe tütarraku vahel.
Tsütokinees võib toimuda mitoosi telofaasiga paralleelselt või pärast seda.
Tsütokinees on raku jagunemisprotsessi etapp, mille käigus kromosoomid , tsütoplasma , organellid ja rakumembraan jagatakse võimaliku...
Tsütokinees on raku jagunemisprotsessi etapp, mille käigus kromosoomid, tsütoplasma, organellid ja rakumembraan jagatakse võimalikult võrdselt kahe tütarraku vahel.
Tsütokinees võib toimuda mitoosi telofaasiga paralleelselt või pärast seda.
Totipotentsus on rakkude arenguline täisvõimelisus, sügoodi, esimeste blastomeeride ja meristeemirakkude võime diferentseeruda mis tahes tüüpi organismiomasteks rakkudeks ja areneda tervikorganismiks.
Sünonüümina kasutatakse ka pluripotentsus. Hans Driesch ja Karl Lashley on kasutanud terminit ekvipotentsiaalsus.
Fibroblast on ekstratsellulaarset maatriksit ja kollageeni sünteesiv rakk. Eritatavad ained on loomse koe tugistruktuuri osad, mis omavad keskset tähtsust haavasulgumises. Fibroblastid on kõige arvukamad sidekoe rakud loomades.
Fibroblastid ja fibrotsüüdid on sama raku kaks vormi. Fibroblastid ja fibrotsüüdid on seotud sidekoe metabolismi ja korrashoiuga, kusjuures fibroblastid on koe korrashoiu ja metabolismi seisukohalt aktiivsemad, fibrotsüüdid vähem aktiivsed rakud. Seni on tendents kutsuda mõlemat rakutüüpi fibroblastideks, kusjuures sõnalõpp "blast" viitab tüvirakule või aktiivses ainevahetuse faasis olevale rakule.
Fibroblastid on morfoloogiliselt heterogeensed, omades palju eri kujusid ja vorme vastavalt raku asukohale ja tegevusele. Kuigi morfoloogiliselt raskesti eristatavad, võivad ektoopiliselt siirdatud rakud säilitada informatsiooni varasema asukoha ja päritolukoe kohta vähemalt mõne generatsiooni vältel. See võib viia tüsistusteni, kui rakkude käitumine on ümbritseva koe omast erinev.
Fibroblastidega samasse rühma kuuluvad ka kõhre ja luukoe rakud. Ühine on neil kollageense materjali eritamine keskkonda. Samuti kuuluvad siia rasvarakud ja silelihasrakud. Eriline nende rakkude puhul on nende omadus muundunda ühest rakutüübist teise, kusjuures kõige muundumisvõimelisem on fibroblast, mis võib muunduda nii luu-, kõhr-, rasv- ja silelihaskoe rakuks. See avaldub näiteks haavade korral, kus epiteelis paiknevad fibroblastid omandavad silelihaskoele omaseid tunnuseid ning aitavad haava koos hoida või kinni tõmmata.
Selliseid muundumisi reguleerib sidekoerakke ümbritsev ekstratsellulaarne maatriks ja selles olevad koefaktorid. Näiteks on võimalik luudest eraldatud fibroblastidega kasvatada nahale kõhre ja lõpuks luukude.
Fibroblastide põhifunktsiooniks on tagada sidekoe struktuurne terviklikkus. See tagatakse pideva ekstratsellulaarse maatriksi prekursoride sekretsiooniga rakuvälisruumi. Fibroblastid sekreteerivad kõikide ekstratsellulaarse maatriksi osade prekursoreid, eelkõige baasaineid ja suurt hulka erinevaid fiibreid. Ekstratsellulaarse maatriksi komponendid määravad sidekoe füüsikalised omadused.
Nagu teised sidekoe rakud, pärinevad ka fibroblastid primitiivsest mesenhüümist. Seetõttu ekspresseerivad nad intermediaarset filamendivalku (tsütoskeleti komponendid, leidub paljudes loomade rakkudes) vimentiini. Selle valgu olemasolu saab kasutada markerina raku mesodermaalse päritolu tuvastamiseks. Tuleb aga tähele panna, et tegu pole ainulaadse omadusega, kuna ka mõnda aega in vitro söötmel kasvatatud epiteeli rakud võivad ekspresseerida vimentiini. Teatud tingimuste olemasolul võivad epiteeli rakud muutuda fibroblastideks. Seda protsessi nimetatakse epiteliaal-mesenhümaalseks üleminekuks (ingl EMT).
Samuti on võimalik vastupidine olukord, kus fibroblast muundub epiteeli rakuks, läbides mesenhümaal-epiteliaal ülemineku (ingl MET). Selle protsessi käigus omandab rakk polarisatsiooni ja lateraalsed ühendused kõrvalolevate rakkudega ning moodustub epiteliaalne rakukiht. See protsess esineb paljudes arengusituatsioonides (näiteks nefroni ja notokordi areng) ning samuti ka haava sulgumises ja tumorigeneesis.
Fibroblastid on suured lamedad rakud ning omavad hargnenud tsütoplasmat, mis ümbritseb lamedat ovaalset rakutuuma, mis sisaldab kahte või enamat tuumakest. Aktiivseid fibroblaste saab eristada tänu nende rohkele karedapinnalisele endoplasmaatilisele retiikulumile. Inaktiivsed fibrotsüüdid on väiksemad, otstes teravneva ovaalse kujuga ja omavad vähem karedapinnalist endoplasmaatilist retiikulumi. Kuigi fibroblastid paiknevad suurel alal eraldi ja hajunult, võtavad nad tiheda asustuse korral tihti paralleelsetesse klastritesse koondudes ühtlase kuju.
Fibroblastid toodavad kollageene, glükosaminoglükaane, retikulaarseid ja elastseid fiibreid, ekstratsellulaarses maatriksis leiduvaid glükoproteiine ja tsütokiini TSLP. Kasvavate indiviidide fibroblastid jagunevad ja sünteesivad baasaineid ekstratsellulaarse maatriksi ja muude koeosade jaoks. Koekahjustus stimuleerib fibrotsüüte ja põhjustab fibroblastide mitoosi. Erinevalt keha õõnsusi vooderdavast epiteelkoest ei moodusta fibroblastid lamedaid rakukihte ega ole polaarselt kinnitunud ühelegi basaalmembraanile, kuigi nad võivad teatud situatsioonides panustada basaalmembraani koostisosadesse. Selle näiteks on subepiteliaalsed müofibroblastid soolestikus, mis võivad sekreteerida α-2 ahelat kandvat laminiini komponenti, mis puudub ainult soolepiirkondades, kust puuduvad ka müofibroblastid. Fibroblastid võivad samuti migreeruda üksikute rakkudena üle söötme, erinevalt epiteeli rakkudest. Kui epiteeli rakud moodustavad organismi katva kihi, siis on fibroblastid ja temaga seotud sidekude see, mis moodustavad suurosa organismi tugistruktuuridest, sealhulgas luud, kõhred ja muud.
Fibroblasti eluiga, mõõdetuna kanaembrüotes, on 57 ± 3 päeva.
Tavalisim fibroblastidega seotud haigus on fibroos, mille käigus tavaliselt armkude moodustav protsess ladestab liigselt armkude keha eri piirkondadesse. See protsess, kuigi ise mitte abnormaalne, võib põhjustada tüsistusi, kui armkude ladestub liigsel hulgal või vales kehapiirkonnas. Selle näiteks on maksa fibroos, mis on esimene samm maksa funktsioonide peatumises. Kuna sidekude ei suuda asendada maksakoe funktsioone, viib see lõpuks maksapuudulikkuseni. On aga ka näidatud, et see protsess on mõnevõrra pöörduv, mis on põhjustanud uuringu antifibrootiliste ravimite väljatöötamiseks.
Hüpertroofiline armistumine on protsess, mille käigus fibroblastid toodavad liigselt kollageeni ning põhjustavad seega muust koest kõrgenenud, kollageenirikka, koloreerunud armi. Selle protsessi puhul on määravaks mehaaniline stress. On näidatud, et regulaarse mehaanilise stressi puhul on fibroblastidel tendents sünteesida rohkelt kasvufaktoreid ja üle minna hüpertroofilist armkude põhjustavaks rakuks.
Samuti on näidatud, et suitsetamine kahjustab kopsude endoplasmaatilist retiikulumi ülal hoidvaid kopsu fibroblaste. Suitsuekstraktiga töödeldud hiirte kopsu fibroblastides muutus redoksreaktsioonide regulatsioon ning rakud suunati apoptoosi. Fibroblastide ja seega ka endoplasmaatilise retiikulumi kadumine põhjustab koe kokkuvarisemist ja sellega seotud terviseriske.
Hiire embrüonaalseid fibroblaste (MEF) kasutatakse tihti toiterakkudena (toodavad tüvirakkude jaoks signaalmolekule) inimese embrüonaalsete tüvirakkude uuringutes. Hiljuti on hakatud MEFe asendama söötmega. Eeliseks on täpselt defineeritud ainete kogused, mis on tuletatud ainult inimese vastavatest ainetest. Selle eeliseks on potentsiaalsete saastete ja tundmatutest kogustest tulenevate vigade vältimine.
Samuti on näidatud, et fibroblastidest on võimalik saada pluripotentsed (rakk, mis on võimeline muunduma kõigiks teisteks rakkudeks peale embrüonaalsete rakkude) tüvirakud. Nimelt on näidatud, et hiire fibroblastidest on võimalik Oct3/4, Sox2, c-Myc, ja Klf4 faktorite lisamisel suunata tagasi pluripotentse tüviraku staadiumisse. Selleks kasutati tüviraku seerumit ning saadud rakke siirdati nii immunodefitsiitsetesse hiirtesse kui ka blastotsüstidesse. Uuringus selgus, et siirdatud tüvirakud põhjustasid suurel hulgal kasvajaid täiskasvanud hiirtes, samas kui blastotsüstid arenesid häireteta.
Huvi pakub ka fibroblastide kasutus Parkinsoni tõve uuringutes. Nimelt on Parkinsoni põdevalt patsiendilt võetud fibroblastid kasutatavad mudelorganismidena, uurimaks Parkinsoni tõve kujunemist raku metabolismiradades. Samuti on võimalik võetud rakke viia pluripotentsesse staadiumisse ning sealt edasi närvirakkudeks, kus haigus väljendub. Samas pole tegu perfektse mudelsüsteemiga, kuna ka fibroblastid ja nende tuletised on tundlikud muid mudeleid mõjutavatele faktoritele.
Munarakk (ka ovotsüüt või ootsüüt) on tütarlapse ja naise organismi haploidne paljunemisrakk.
Munaraku diameeter on 120 µm (s.o 0,12 mm). See on inimese ja kõigi teiste imetajate rakkudest kõige suurema läbimõõduga rakk. Ainuke rakk, mis on palja silmaga nähtav (närvirakud oma pikkade aksonjätketega ületavad pikkuses kõiki teisi organismi rakke). Kuna munarakk on nii suur, ei suuda ta ise aktiivselt liikuda. See omadus on otse vastupidine võrreldes ülimobiilse seemnerakuga. Munarakk on kerajas, tema keskel on rakutuum ja ta on kaetud mitmete kestadega. Munarakkudes on haploidne kromosoomistik. Munarakkude ainevahetus on suhteliselt väheaktiivne. Nii väheneb risk kahjulike muutuste tekkeks sugurakkudes. Munarakud tekivad munasarjades. Seda protsessi nimetatakse ovogeneesiks. Kõik munarakud on moodustunud juba lootelise arengu perioodil ja naise elu jooksul neid juurde ei moodustu. Vastsündinu munasarjades on ligikaudu 400 000 munarakku, millest valmib elu jooksul umbes 400. See on 0,1% kogu naise munarakkude kogusest. Viljastatud munarakust, ühest ainsast rakust saab alguse kõikide imetajate ontogenees. Imetajate munaraku avastas 1827. aastal embrüoloogia- ja arengubioloogiaalase uurimistöö käigus Eestist pärit ja Tartu Ülikoolis õppinud teadlane Karl Ernst von Baer.
Sulgrakkudeks nimetatakse taimede spetsialiseerunud rakke, mis paaridena ääristavad õhulõhesid. Nad osalevad taime gaasivahetuses, muutes õhulõhe avatust erinevates taimekudedes. Nii toimivadki sulgrakud süsihappagaasi (CO2) ja veeauru väravatena.

Sulgrakke leidub lehtedes, vartes ja teiste gaasivahetusega seotud organite epidermises. Enamikul taimedel paiknevad õhulõhed lehtede alumisel küljel, aga on ka taimi, millel on õhulõhed mõlemal või ainult lehe pealmisel küljel. Kui mullas on piisavalt vett, siis õhulõhed avanevad, sest sulgrakud täituvad veega, paisuvad ja neis olev turgorrõhk suureneb. Veepuuduse korral vähenevad veesisaldus ja turgorrõhk sulgrakkudes ning õhulõhe sulgub. Nii minimeerib taim veekaotust.
Sulgrakud reguleerivad gaasivahetust taime ja väliskeskkonna vahel: hapniku ja vee väljutamist ning süsihappegaasi omastamist. Taimetüübist sõltumata toimub õhulõhede sulgemine ja avamine samal põhimõttel. Sulgrakkudel on samuti kaitsefunktsioon, sest bakterid, saasteained ja seened saavad läbi õhulõhede taime siseneda. Kui taim sellise ohu avastab, sulevad sulgrakud kiirelt õhulõhe. Õhulõhede reguleerimine sulgrakkudega on üks viisidest, kuidas taim tuleb muutuva keskkonnaga toime.
Sulgrakkude uurimise mudelorganismiks on tihti harilik müürlook (Arabidopsis thaliana).

Taime gaasivahetuse tähtsus seisneb eelkõige taime varustamises süsihappegaasiga. Tänu õhulõhedele saavad taimed piisavalt süsihappegaasi, säilitades võimaluse neid avasid sulgeda. Kui gaasivahetus toimuks läbi taime rakuseinte, siis peaksid need õhemad olema. See aga muudaks taime ebastabiilsemaks. Lisaks suureneks taimest aurustunud vee hulk, kuna taimel poleks mingit võimalust enda veekaotust vähendada.
Vee aurustumine võimaldab taimel enda temperatuuri alandada. Vee aurumine jahutab lehte ning seal olevad ensüümid ei lagune nii kiirelt. Lehtedest aurustuv vesi põhjustab ka vee liikumist juurtest lehtedeni läbi ksüleemi. Vees on lahustunud erinevad mineraalained, mis juurte kaudu pinnasest taime on jõudnud. Tänu vee liikumisele jõuavad need ained ka taime maapealsetesse osadesse. Seega täidavad sulgrakud ja õhulõhe samu funktsioone, mis inimestel süda, suu, nina ja nahk.

Sulgrakul on tuum, vakuoolid, mitokondrid ja kloroplastid. Viimastesse koguneb päeva jooksul tärklis, mis õhulõhede avanedes öö jooksul väheneb. Vakuooli maht kogu raku mahust on väga muutuv suurus, sest avanenud õhulõhe sulgrakkudes võib vakuooli maht moodustada 90% kogu raku mahust. Sulgrakkude sisemine sein on paksem kui välimine. Seetõttu paisuvadki nad väljapoole, tõmmates sisemisi külgi üksteisest eemale. Sulgrakud on nagu kogu epidermis kaetud kutiikulaga, mille üks ülesandeid on veeaurustumist vähendada. Sulgrakke kattev kutiikula erineb tavaliste rakkude omast, sest see laseb vett paremini läbi.
Õhulõhe avanemise ja sulgumise kutsub esile turgorrõhu muutus teda ümbritseva kahe sulgraku sees. Õhulõhe sulgub, kui sulgrakkudes on vähe vett, ja avaneb, kui seal on palju vett. Vesi liigub rakkudesse tänu osmootse rõhu kasvule rakus. Rakus olev veepotentsiaal aga langeb. Selleks peab rakus olema osmootselt aktiivsete ainete kontsentratsioon suurem kui rakust väljas. Seda saavutatakse tänu sulgrakkude plasmamembraanis paiknevatele ATPaasidele, mis pumpavad prootoneid sulgrakust välja. Membraan polariseerub, tekib elektrokeemiline gradient, mille abil saadakse kaaliumioonid sulgrakku. Laengu tasakaalustamiseks liiguvad rakku ka anioonid, milleks on enamasti kloriidioonid, ja fotosünteesi produktidena koguneb rakku ka malaat. Õhulõhed suletakse ATPaasi inhibitsiooni kaudu. Õhulõhede avatust mõjutavad valguse hulk, selle kvaliteet, vee kättesaadavus ja süsihappegaasi kontsentratsioon õhus. Näiteks oleksid sulgrakud paisunud, kui neid valgustada sinise valgusega, anda taimele piisavalt vett ja süsihappegaasi. Lisaks mõjutavad avatust ka erinevad fütohormoonid (abtsiishape ja auksiin).

Taimed taluvad stressi tihti just veepuuduse tõttu, mida põhjustavad põuad ja liigsed soolad. Piiratud vee kättesaadavus põhjustab kahju nii loodusele kui ka põllumajandusele. Taimede põuaga toimetulekut mõjutavad mitmed koostoimivad mehhanismid. Veevaesetes kohtades kasvavad taimed on arenenud veepuudusega toime tulema. Osad samblad taluvad näiteks dessikatsiooni (olukord, kus taimes ja atmosfääris olev niiskussisaldus on võrdne). Leidub kõrbetaimi, kes veedavad kuivaperioodi seemnetena. Samuti kasvatatakse endale hästi sügavaid juuri, hoitakse vett spetsiaalsetes veereservuaarides või loobutakse suurtest lehtedest. Vee kättesaadavuse langedes suunab taim enda ressursse eelistatult juurte kasvatamisse.
Abstsiishapet (ABA), mis on üks taimehormoon, hakatakse taimes tootma stressivastusena veepuudusele. ABA mõjul suleb taim õhulõhed, mis omakorda vähendab transpiratsiooni.
Tulevikus loodetakse luua taimi, mis oskaksid paremini vett kasutada ja oleksid tänu sellele vastupidavamad põudade suhtes.
C3- ja C4-taimed sulgevad oma õhulõhed pimedas ja avavad valges. Nende sulgrakkude avanemist põhjustavad ka sinine ja punane valgus. CAM-taimed aga avavad õhulõhesid just pimedas, et minimeerida õhulõhedest aurustuva vee hulka. Nad seovad süsihappegaasi öösiti, et seda kasutada päeval, kui päikesevalguses toimub fotosüntees. CO2 seotakse orgaaniliste molekulidena, näiteks malaadina.
Kui süsihappegaasi kontsentratsioon õhus kasvab, siis õhulõhed ahenevad, sest ka vähemal määral avatuna on võimalik kätte saada vajalik kogus süsihappegaasi. Veel suletakse õhulõhesid, kui taimel on veepuudus. Nii vähendatakse veekadu läbi transpiratsiooni. Põuaajal hakkab taim tootma abtsiishapet, mis sunnib taimi õhulõhesid sulgema. Õhulõhede avatust võivad mõjutada ka teised taimehormoonid. Samuti suletakse õhulõhed siis, kui õhus on palju osooni, et kaitsta taime sisemisi kudesid oksüdatiivse stressi eest.
Õhulõhe on auk epidermis, mida ümbritsevad sulgrakud. Sulgrakud mõjutavad õhulõhede juhtivust ehk seda, kui palju vett aurustub lehest välja. Pingutunud sulgrakkude puhul on õhulõhed lahti, nende juhtivus suur ja takistus väike. Õhulõhed saavad oma funktsiooni täitmist tagada ainult tänu sulgrakkude tööle. Seetõttu on võimalik jaotada õhulõhesid vastavalt lõhe ümber paiknevatele sulgrakkudele.
Sulgrakud võtavad vastu ning töötlevad keskkonnast tulevaid biootilisi ja abiootilisi signaale ning endogeenseid signaale. Väliskeskkonnast saadud signaalideks on näiteks valgus, õhuniiskus, süsihappegaasi ja osooni kontsentratsioon, temperatuur, kuivus ning feromoonid. Taim ise sünteesib fütohormoone. Signaalidest tulenev info kutsub esile vastuse sulgrakkudes, mille tagajärjel õhulõhed avanevad või sulguvad. Just nende signaalide levik määrab, kui kiiresti kaotab taim kuivaperioodil vett. Abtsiishape põhjustab Ca2+ ioonide tõusu sulgrakkudes ning muudab vastava molekuli retseptoreid tundlikumaks. See aktiveerib S- ja R-tüüpi anioonikanalid (esimene on teisest aeglasema, aga ühtlasema anioonivooluga) ning K+-kanali, mis transpordivad vastvad ioonid sulgrakust välja. See omakorda põhjustab vee liikumise sulgrakkudest välja, mille tagajärjel turgorrõhk nendes väheneb ja õhulõhed sulguvad.
Sulgrakkude ja õhulõhede arengut mõjutavad nii geenid kui ka keskkonnasignaalid. Sulgrakkude paiknemise tihedust mõjutavad keskkonnasignaalid, muuhulgas ka süsihappegaasi kontsentratsioon õhus. Kõrgema CO2 taseme korral kujuneb lehtedel vähem õhulõhesid
Tüvirakk (ld cellula praecursoria, mitm cellulae praecursoriae) on hulkraksete organismide erinevates kudedes leiduvate diferentseerumata paljunemisvõimeliste algrakkude tüüp. Tüvirakud võivad muunduda ehk diferentseeruda spetsiaalse funktsiooniga rakkudeks või jaguneda mitoosi teel samasugusteks tüvirakkudeks.
Imetajatel on kirjeldatud kahte tüüpi tüvirakke: embrüonaalseid ja täiskasvanud tüvirakke. Täiskasvanud organismis uuendavad tüvirakud kudesid ehk on osa keha parandamise süsteemist. Teadlased on õppinud tüvirakke kunstlikult kasvatama ja kindla funktsiooniga rakkudeks diferentseerima.
Täiskasvanud inimese kehas on autoloogsete tüvirakkude eraldamiseks neli kohta:
Arvatakse, et tüvirakkudel on palju sarnasusi vähirakkudega.
Taimedel on sarnase funktsiooniga rakkudeks algkoe ehk meristeemi rakud.

Embrüonaalsed tüvirakud pärinevad blastotsüsti ehk lootepõiekese sisemisest rakumassist. Need on pluripotentsed ja annavad alguse kolmele põhilisele lootelehele: ektodermile, endodermile ja mesodermile. Nad võivad diferentseeruda enam kui kahesajaks täiskasvand organismis esinevaks rakutüübiks. Pea kõik tüvirakkudega seotud uuringud on läbi viidud kas hiire (mES) või inimese embrüonaalsete tüvirakkudega (hES). Need vajavad diferentseerumata oleku säilitamiseks väga erinevaid tingimusi. Inimese embrüonaalseid tüvirakke saab tavalistest rakkudest eristada mitmete spetsiifiliste transkriptsioonifaktorite ekspressiooni ja raku pinnaretseptorite järgi.
Embrüonaalsed tüvirakud vajavad diferentseerumiseks spetsiifilisi signaale. Kui selliseid rakke süstida teise organismi, siis hakkavad rakud diferentseeruma paljudeks eri rakkudeks, põhjustades nii teatud tüüpi kasvaja, mida nimetatakse teratoomiks.
Embrüonaalsetele tüvirakkudele omistatakse biomeditsiinis tänapäeval erilist tähtsust. Need on oma pluripotentsuse tõttu potentsiaalseks ravimeetodiks regeneratiivmeditsiinis ja haiguse või vigastuse tagajärjel kahjustatud kudede taastamisel.
Inimese lootelt saadud embrüonaalsete tüvirakkude uurimisobjektina kasutamisele on esitatud eetilisi vastuväiteid põhjendusega, et selliste tüvirakkude saamiseks lõhutavat blastotsüsti (s.o embrüo, milles ei ole veel üle 150 raku) võib pidada inimeseks.
Täiskasvanud tüvirakud ehk somaatilised tüvirakud ehk keha tüvirakud on diferentseerumata rakud, mis esinevad teatud koe diferentseerunud rakkude hulgas ning on enamasti multipotentsed. Hoolimata nimest leidub neid ka lastel ja sündimisel saab neid eraldada ka nabaväädist. Pluripotentsed täiskasvanud tüvirakud on haruldased, kuid neid leidub mitmes koes. Luuüdis leidub rohkelt täiskasvanud tüvirakke. Luuüdis leiduvate tüvirakkude arv kahaneb organismi vananedes. Täiskasvanud tüvirakke on kasutatud mitmete seljaajuvigastuste, maksatsirroosi ja kroonilise jäsemete isheemia ravimiseks. Lisaks on neid kasutatud leukeemia ja muude sarnaste luu- ja verevähkide ravimiseks. Samuti kasutatakse täiskasvanud tüvirakke veterinaarias kõõluste ja sidemete vigastuste ravimiseks hobustel. Täiskasvanud tüvirakkude kasutamine pole nii vastuoluline kui embrüonaalsete tüvirakkude kasutamine, sest täiskasvanud tüvirakkude saamiseks pole vaja embrüot lõhkuda.
Multipotentseid tüvirakke leidub ka loote amnioni vedelikus. Need tüvirakud on väga aktiivsed, jagunevad kiiresti ja pole tumorogeensed. Rooma-Katoliku Kiriku õpetus keelab embrüonaalsete tüvirakkude kasutamise, kuid Vatikani ajaleht Osservatore Romano nimetas amniootilisi tüvirakke "meditsiini tulevikuks". 2009. aastal avati esimene amniootiliste tüvirakkude pank, mis teeb koostööd mitmete haiglate ja ülikoolidega üle maailma.
Teatud tüüpi tüvirakud (CB-SC), mis on saadud nabaväädi verest, on multipotentsed: neil on nii embrüonaalsed kui hematopoeetilised omadused. Fenotüübiline klassifikatsioon näitab, et nendel rakkudel on embrüonaalse raku markerid (transkripitsioonifaktorid OCT-4 ja Nanog) ja raku elufaasile iseloomulikud embrüonaalsed antigeenid. Nabaväädi vere tüvirakkudel on potentsiaal ravida autoimmuunhaigusi.
Indutseeritud pluripotentsed tüvirakud saadakse täiskasvanud organismi diferentseerunud rakkude ümberprogrammeerimisel nii, et nad omandavad pluripotentsuse. Nii saab näiteks hiire naharakkudes indutseerida tüviraku omadusi ja see rakk võib omakorda diferentseeruda spetsialiseerunud rakuks, näiteks munarakuks.
Teadlaste arvates on tüvirakkudel potentsiaal drastiliselt muuta tänapäeva meditsiini. Juba praegu suudetakse nende abil ravida leukeemiat ja mitmeid vere- ja luuvähi tüüpe. Loodetakse, et tulevikus saab tüvirakkudega hakata ravima mitmeid haigusi, nagu vähki, Parkinsoni tõve, seljaajuvigastusi, polüskleroosi ja lihaste vigastusi. Tüvirakkude kasutamisel on siiski risk, et need võivad moodustada kasvajaid. Kontrollimatu rakujagunemise korral võivad need kasvajad muutuda ka pahaloomuliseks. Isegi kui tüvirakud on võetud patsiendilt endalt, võib tekkida kasvaja, sest mitokondriaalses DNAs toimuvad mutatsioonid palju tihedamini kui inimese genoomis.
Lüsosoom on üks rakuplasmas asetsevatest rakuorganellidest, ühekordse rakumembraaniga ümbritsetud põieke, mille sees paiknevad ensüümid lahustavad rakusiseseid valke, makromolekule ja rakustruktuure.

Lüsosoome on leitud loomarakkudest, nende esinemine pärmseentes ja taimedes on vaidluse all.
Lüsosoomid avastas Belgia tsütoloog Christian de Duve 1949. aastal.
Lüsosoomi suurus võib olla 0,1–1,2 μm.
Embrüonaalsed tüvirakud on pluripotentsed tüvirakud, mis on saadud embrüo varajase staadiumi blastotsüsti sisemisest rakumassist. Inimese embrüo jõuab blastotsüsti staadiumisse 4–5 päeva pärast viljastumist, koosnedes ligikaudu 50–100 rakust. Inimese embrüonaalsete tüvirakkude saamine püstitab palju eetilisi probleeme, sest viljastatud munarakk hävineb sisemise rakumassi isoleerimisel.

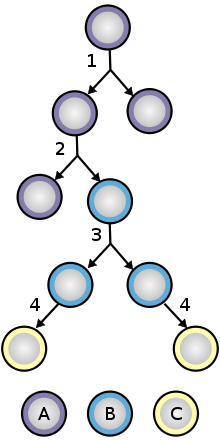
Teadustöös enimkasutatavate inimese ja hiire embrüonaalsete tüvirakkude diameeter on vastavalt ligikaudu 14 ja 8 μm. Embrüonaalseid tüvirakke iseloomustab nende kaks eriomadust:
Embrüonaalsed tüvirakud on pluripotentsed, mis tähendab, et nad suudavad diferentseeruda kõikideks primaarseteks lootelehtedeks: välimine (ektoderm), keskmine (mesoderm) ja sisemine (endoderm). Täiskasvanud inimese kehas kuulub igasse lootelehte rohkem kui 220 rakutüüpi. Pluripotentsus eristabki embrüonaalsed tüvirakke täiskasvanu (somaatilistest) tüvirakkudest, sest embrüonaalsed tüvirakud panevad aluse kõigile keharakutüüpidele, kuid somaatilised tüvirakud on multipotentsed ehk nende diferentseerumisvõime on piiratud.
Spetsiifilises kasvukeskkonnas säilitavad embrüonaalsed tüvirakud oma piiramatu jagunemisvõime. See võimaldab embrüonaalseid tüvirakke kasutada edukalt teadustöös ja loodetavasti ka tuleviku meditsiinilises taastusravis.
Arvatakse, et embrüonaalsete tüvirakkude plastilisust ja potentsiaali piiramatuks paljunemiseks saab kasutada taastusravis ja vigastatud või haigete kudede asendamiseks. Meditsiinis võiks pluripotentsete tüvirakkude abil ravida palju vere ja immuunsüsteemiga seotud haigusi ja häireid, vähkkasvajaid, laste diabeeti, Parkinsoni tõbe ja selgroovigastusi. Lisaks tüvirakuteraapia eetilistele probleemidele, on teiselt inimeselt (allogeensel) tüvirakkude siirdamisel takistavaks teguriks ka doonori ja vastuvõtja sobimatus. Koesobivuse probleemi lahendamisel võivad abiks olla inimese enda somaatiliste tüvirakkude kasutamine, terapeutiline kloonimine, tüvirakupangad või kindlate faktoritega reprogrammeeritud somaatiliste rakkude kasutamine (indutseeritud pluripotentsed tüvirakud). Embrüonaalseid tüvirakke kasutatakse ka inimese varajase arengu ja geneetiliste haiguste uurimiseks ning in vitro süsteemina toksikoloogilistes katsetustes.
1964. aastal eraldati teratokartsinoomist, mis oli sugurakkudest tekkinud kasvaja, kindel rakutüüp. Need teratokartsinoomist eraldatud rakud paljunesid ja kasvasid rakukultuuris nagu tüvirakud ja on tänapäeval tuntud kui embrüonaalse vähi rakud. Sarnase välimuse ja diferentseerumise potentsiaali (pluripotentsus) tõttu hakati embrüonaalse kartsinoomi rakke kasutama hiire varajase arengu in vitro mudelina. Teratokartsinoomi arengu jooksul tekivad embrüonaalse kartsinoomi rakkudes geneetilised mutatsioonid ja ebanormaalne karüotüüp. Sellised geneetilised kõrvalekalded tekitasidki vajaduse normaalsete pluripotentsete rakkude eraldamiseks blastotsüsti sisemisest rakumassist.
1981. aastal eraldati esimest korda hiire embrüonaalsed tüvirakud kahes erinevas teadustöörühmas. Martin Evans ja Matthew Kaufman Cambridge'i Ülikooli geneetika osakonnast avaldasid juulis uue protseduuri, mis võimaldas kasvatada hiire embrüoid emakas, suurendades rakkude arvu ja saades embrüost embrüonaalsed tüvirakke. Gail R. Martin San Francisco California Ülikooli anatoomia osakonnast avaldas oma artikli detsembris ja mõtles välja termini "embrüonaalne tüvirakk". Ta näitas, et embrüoid saab ka in vitro kasvatada ning hiljem saab neist ka embrüonaalseid tüvirakke. 1998. aastal toimus aga läbimurre, sest James Thomsoni juhitud Wisconsin-Madisoni Ülikooli teadlased olid esimesed, kes töötasid välja metoodika inimese embrüonaalsete tüvirakkude isoleerimiseks ja kasvatamiseks rakukultuuris.
Inimese embrüonaalsete tüvirakkude saamine. In vitro viljastamise protseduuris kasutatakse algselt mitmeid munarakke ja tekkinud embrüotest valitakse välja parimad. Ülejäävaid embrüoid, mida kliiniliselt ei kasutata või mis on sobimatud implantatsiooniks patsienti, saab doonori nõusolekul annetada. Nendest annetatud embrüotest, mis muidu hävitataks, saadaksegi inimese embrüonaalsed tüvirakud. Blastotsüstistaadiumis olevast embrüost eraldatakse sisemine rakumass, kasutades mehaanilist lahkamist ja immunokirurgiat. Saadud sisemine rakumass pannakse kasvama abirakkudele ehk toiterakkudele. Sisemise rakumassi rakud kinnituvad ja jagunevad veelgi, moodustades inimese embrüonaalsed diferentseerumata rakud. Neid rakke toidetakse iga päev ja passeeritakse kas ensümaatiliselt või mehaaniliselt iga nelja kuni seitsme päeva tagant. Diferentseerumise tekkimiseks eraldatakse embrüonaalsed tüvirakud abirakkudelt, et moodustuksid embrüonaalsed kehad, kasutades selleks seerumit või muid diferentseerumist soodustavaid meetodeid.
Hiire embrüonaalsete tüvirakkude saamine. Embrüonaalsed tüvirakud eraldati emase doonorlooma varajase embrüo sisemisest rakumassist. Martin Evans ja Matthew Kaufman teatasid meetodist, mis võimaldab hiire embrüo implantatsiooni edasi lükata ja seega kasvatada sisemist rakumassi. Selle protsessi käigus eemaldatakse doonorema munasarjad ja hormoonkeskkonna muutmiseks manustatakse progesterooni, mistõttu embrüod ei kinnitu emakas. Embrüod võetakse ära pärast 4–6 päeva sellises emakasiseses keskkonnas kasvamist ja pannakse kasvama in vitro keskkonda, kuni sisemine rakumass moodustab "munakujulise" struktuuri, mis seejärel muudetakse omakorda üksikrakuliseks ja külvatakse mitomütsiin C-ga (fibroblastide mitoosi vältimiseks) töödeldud fibroblastidele. Üksikrakuliselt kasvatades tekivad klonaalsed rakuliinid. Evans ja Kaufman tõestasid, et sellises rakukultuuris kasvanud hiire rakud suudavad moodustada nii teratoomi kui ka embrüonaalseid kehi, samuti in vitro diferentseeruda, mis kõik kinnitab, et need rakud on pluripotentsed.
Gail Martin eraldas ja kasvatas hiire embrüonaalseid tüvirakke teisiti. Ta eemaldas doonorema embrüod umbes 76 tundi pärast kopulatsiooni ja kasvatas neid öö läbi seerumit sisaldavas söötmes. Kasutades mikrokirurgiat, eraldas ta järgmisel päeval hiire hilise blastotsüsti sisemise rakumassi. Kasvatas seda eraldatud sisemist rakumassi spetsiaalsel söötmel ja mitootiliselt inaktiveeritud fibroblastidel. Nädala pärast ilmusid rakukolooniad, mis kasvasid hästi koekultuuris ja olid pluripotentsete omadustega. Seda näitas rakkude võime moodustada teratoome, diferentseeruda in vitro ja moodustada embrüonaalseid kehi. Martin viitas neile rakkudele kui embrüonaalsetele tüvirakkudele.
Tänapäeval teatakse, et koekultuuris rutiinselt kasutatav seerum sisaldab luu morfogeneetilist valku (BMP) ja toiterakud toodavad leukeemiat inhibeerivat faktorit (LIF), mis on vajalikud hiire embrüonaalsete tüvirakkude diferentseerumise takistamiseks. Need faktorid on äärmiselt olulised hiire embrüonaalsete tüvirakkude efektiivseks kasvatamiseks. Samuti on näidatud, et embrüonaalsete tüvirakkude isoleerimise efektiivsus sõltub hiireliinist. Tänapäeva teadustöös kasutatakse hiire embrüonaalseid tüvirakke transgeensete hiirte, kaasa arvatud knock-out hiirte, tegemiseks.
Inimese embrüonaalsete tüvirakkude loomine on palju keerulisem ja seisab silmitsi eetiliste probleemidega. Seega on paljud teadustöörühmad lisaks inimese embrüonaalsete tüvirakkude uurimisele pühendunud ka indutseeritud pluripotentsete tüvirakkude loomisele.
Ajakirja Nature Medicine internetiväljaanne avaldas 24. jaanuaril 2005 uurimuse, mis väitis, et inimese embrüonaalsed tüvirakud, mida kasutatakse föderaalseadusega rahastatud teadustöös, on saastunud inimesele mitteomaste molekulidega, mis on tulnud rakkude kasvukeskkonnast. Hiire ja teiste loomade rakkude kasutamine abirakkudena aktiivselt jagunevate rakkude pluripotentsuse säilitamiseks on aga väga levinud meetod. San Diego California Ülikooli teadlaste sõnul seadis embrüonaalsete tüvirakkude kasutamise inimeses ohtu söötmes leiduv inimesele mitteomane siaalhape.
Seevastu väljaande Lancet Medical Journal internetiversioon avaldas 2005. aasta 8. märtsil üksikasjaliku ülevaate, kuidas täielikult raku- ja seerumivabadel tingimustel saadi inimese embrüost uus tüvirakuliin. Need rakud suutsid rohkem kui kuus kuud olla diferentseerumata prolifereeruvas olekus ning moodustada kõige kolme lootelehte rakke nii in vitro tingimustes kui ka teratoomides. Need omadused säilisid edukalt (rohkem kui 30 passeerimisel) ka loodud rakuliinidel.
Mitmed teadustöörühmad tegelevad embrüonaalsetest tüvirakkudest saadud diferentseerunud rakkude doonor-vastuvõtja mittesobivuse vähendamisega nende siirdamisel patsienti. Üheks võimaluseks oleks patsiendiga geneetiliselt identsete embrüonaalsete tüvirakkude tegemine, kasutades terapeutilist kloonimist.
Alternatiivseks võimaluseks mittekloonitud embrüonaalsete tüvirakkude teraapias on paljude võimalikult erinevate geneetilise taustaga tüvirakuliinide tegemine. Suurima sarnasusega liini kasutamine võimaldaks kohandada ravi vastavalt patsiendile, langetades mittesobivuse riski.
I faasi kliinilised katsetused embrüonaalsetest tüvirakkudest saadud oligodendrotsüütide (aju ja seljaaju rakutüüp) transplantatsioonil seljaajuvigastusega isikutele toimusid 2009. aasta 23. jaanuaril. Need said USA toidu- ja ravimiameti heakskiidu ning sellest sai seega maailma esimene inimese embrüonaalsete tüvirakkude inimkatse. Uuringud, mis viisid selle teadusliku saavutuseni, teostasid Hans Keirstead ja tema kolleegid California Ülikoolis Irvine'is.
Nende sooritatud eksperimendis diferentseeriti inimese embrüonaalseid tüvirakke oligodendrotsüütideks ja kasutati transplantatsiooniks. Tulemused näitasid liikumisaktiivsuse taastumist seljaajuvigastusega rottides seitse päeva pärast inimese diferentseeritud tüvirakkude transplantatsiooni. Antud I faasi kliinilises uuringus valiti umbes kaheksa kuni kümme parapleegikut (mõlemapoolselt halvatud), kelle vigastused tekitati vähem kui kaks nädalat enne katsetuste algust, et rakke saaks süstida enne võimaliku armkoe teket. Teadlased rõhutasid, et antud uuringu puhul ei oodatudki patsientide täielikku tervenemist ja kogu liikuvuse taastumist. Uurijad väitsid saadud tulemuste põhjal, et müeliintupe taastumine ja liikuvuse suurenemine on võimalikud.
Esimene teostatud uuring oligi põhiliselt protseduuride ohutuse testimiseks ja oodatud tulemuste korral võib see viia edasiste uuringuteni, kuhu kaasatakse raskemate puuetega inimesi. Uuringud pandi ootele 2009. aasta augustis, kui mitmest käsitletud rotist leiti väike hulk mikroskoopilisi tsüste, kuid keeld tühistati 2010. aasta 30. juulil.
Esimese inimpatsiendi raviks kaasati ja manustati embrüonaalseid tüvirakke Atlantas 2010. aasta oktoobris. Tüvirakuteraapia eestvedaja Geron Corporation arvates kulub tüvirakkudel jagunemiseks mitu kuud ning enne pole võimalik hinnata teraapia edukust või läbikukkumist.
23. augustil 2006 avaldas ajakirja Nature teaduslik internetiväljaanne Robert Lanza kirjutise, mis väitis, et tema meeskond on leidnud võimaluse embrüonaalsete tüvirakkude eemaldamiseks embrüot lõhkumata. Selline tehniline areng võimaldas teadlastel teha tööd uute embrüonaalsete tüvirakkudega, kasutades USA-s avaliku sektori finantseeringuid, samal ajal kui föderaalne rahastamine oli piiratud ja sai kasutada ainult embrüonaalseid tüvirakke, mis olid eraldatud enne 2001. aasta augustit. 2009. aasta märtsis piirang tühistati.
On teada, et viies diferentseerunud rakkudesse kolm geeni (Oct4, Sox2 ja Klf4), saab teha embrüonaalsete tüvirakkude sarnaseid pluripotentseid tüvirakke. Need geenid "reprogrammeerivad" diferentseerunud rakud pluripotentseteks tüvirakkudeks, võimaldades pluripotentsete tüvirakkude teket embrüot kasutamata. Kuna embrüonaalsete tüvirakkude eetilised probleemid on just seotud nende saamisega embrüotest, usutakse, et reprogrammeerimine "indutseeritud pluripotentseteks tüvirakkudeks" võib olla sobivam lahendus. Nii inimese kui ka hiire rakke saab selle meetodiga reprogrammeerida, saades embrüot kasutamata pluripotentseid tüvirakke.
Arvatakse, et patsiendispetsiifilisi embrüonaalseid tüvirakuliine saaks kasutada rakulises asendusravis. Samuti saaks indutseeritud pluripotentsuse metoodika abil arendada embrüonaalsete tüvirakkude liine, mis on saadud erinevate geneetiliste haigustega patsientidelt ja saada seega hindamatu mudel nende haiguste uurimiseks.
Esimene märk sellest, et indutseeritud pluripotentsete rakkude teraapia võib viia uue ravini, oli 6. detsembril 2007 ajakirjas Science avaldatud artikkel, kus Rudolf Jaenischi juhitud uurimisgrupp kasutas seda hiirte sirprakulise aneemia ravis.
16. jaanuaril 2008 teatas California ettevõte Stemagen, et nad lõid täiskasvanult saadud naharakkudest esimese kloonitud inimembrüo. Neist embrüotest oleks võimalik võtta patsiendiga sobivaid embrüonaalseid tüvirakke.
Mitmed teadusgrupid on hakanud embrüonaalseid tüvirakke kasutama inimese geneetiliste häirete mudelina. Seda on tehtud rakke geneetiliselt manipuleerides või viimasel ajal ka kasutades pigem implantatsioonieelse geneetilise diagnoosiga (PGD) rakke. Selline lähenemine võib olla väärtuslik erinevate haiguste (nt fragiilse X-i sündroom, tsüstiline fibroos) ja ka nende geneetiliste haiguste uurimises, millel ei ole veel usaldusväärset mudelsüsteemi.